Tomografía computada cuantitativa
tridimensional (QCT-3D) para la evaluación
de masa y arquitectura ósea
María Loreto Reyes G1, Cristian García B2
Three dimensional quantitative computed
tomography (qct -3d) for the assessment
of bone mass and architecture
¹Departamento de Pediatría, Programa de Metabolismo Óseo,
Facultad de Medicina, Pontificia Universidad Católica de Chile.
2Departamento de Radiología, Facultad de Medicina,
Pontificia Universidad Católica de Chile.
Correspondencia a:
María Loreto Reyes G.
Departamento de Pediatría, Programa de Metabolismo Óseo,
Facultad de Medicina, Pontificia Universidad Católica de Chile.
Fono-Fax: (56-2) 354 8085
E-mail: mlreyes@med.puc.cl
Recibido: 27 Agosto de 2008
Aceptado: 02 Diciembre de de 2008
From a clinical point of view, three dimensional quantitative computed tomography has not replaced dual energy X ray absortiometry (DEXA) as the test of choice to assess bone mass in adults and children. This is particularly true in postmenopausal osteoporosis and in patients without significant disturbances of body size. However, in particular diseases such as skeletal dysplasia, Turner syndrome and other endocrine diseases associated to stunting, QCT-3D can provide accurate information about bone health. It is also informative when the trabecular/cortical bone ratios are altered. QCT-3D is widely used for research purposes and it became available in Chile recently.
Introducción
La evaluación de la masa ósea es una necesidad cada día mas frecuente, tanto en la edad adulta como en la pediátrica. El objetivo principal que debe cumplir este procedimiento es expresar de la manera más real posible, cual es el riesgo de un paciente de padecer o no una fractura ósea1.
El riesgo de sufrir una fractura se correlaciona directamente con la densidad mineral ósea areal medida por DXA; sin embargo, esta información solo explica un 60% de ese riesgo. Otras variables responsables del porcentaje restante tienen que ver con las características de la matriz ósea, la proporción entre hueso trabecular y cortical, y la geometría del hueso. En este último punto son importantes el largo del hueso, el ancho total, así como el diámetro interno (endosteal) y externo (periosteal)2.
Para mejor comprensión de estos conceptos, se ha propuesto definir la densidad mineral ósea en tres niveles distintos. El primero y más preciso, es el concepto de densitometría de material o de tejido, que se refiere a la densidad del hueso trabecular y cortical por separado, y a su microarquitectura. Este nivel puede ser evaluado adecuadamente mediante una biopsia de hueso calcificado o con histomorfometría ósea. El segundo nivel se refiere al concepto de densitometría compartamental, que se expresa en la evaluación de la densidad mineral del compartimento cortical y trabecular por separado y la macroarquitectura ósea. Este nivel puede ser bien evaluado mediante la tomografía computada cuantitativa. Finalmente, el último nivel y el menos preciso, es la densidad total o de órgano, que es la densidad mineral ósea cortical y trabecular en conjunto, sin información sobre la arquitectura. Este es el nivel propio de la medición por DXA3.
La densidad medida por DXA, resulta del contenido mineral calculado para el área proyectada por los rayos X al atravesar el cuerpo en estudio. De esta manera, la densitometría medida por DXA es directamente proporcional al tamaño corporal. Existe una correlación significativa, tanto en adultos como en niños, entre la densitometría areal medida y la talla con el Índice de masa corporal4. De esta manera, en el caso de cuerpos pequeños o livianos, con DXA obtendremos un valor densitométrico menor que si se mide un cuerpo de mayor tamaño, aun cuando la densidad real o volumétrica de los huesos sea idéntica en ambos casos. Adicionalmente, DXA nada nos dice sobre las características geométricas o de macro o micro arquitectura ósea5.
Las limitaciones mencionadas pudieran no ser tan importantes en la mayoría de los adultos promedio o con patologías comunes como la osteoporosis postmenopáusica. Sin embargo, en la edad pediátrica, donde la asociación entre osteoporosis y talla o peso bajo es frecuente, DXA aparece como una herramienta limitada5,6. Recientemente, Wren et al, en una población de 200 niños sanos y enfermos, muestra que DXA sobrediagnostica osteoporosis en niños con respecto a QCT (76 de 400 versus 25 de 400). Esto fue especialmente notorio en el grupo con talla menor al percentil 5. Usando QCT como patrón de oro, la especificidad de DXA fue 94% en niños sanos comparada con un 74 % en niños enfermos7. En el caso de los adultos, la Sociedad Internacional de Densitometría Clínica (ISCD), en su último consenso, ha concluido que su uso en cadera puede ser clínicamente relevante, por ser un importante sitio de fractura; sin embargo, se reserva la recomendación de su uso en la práctica clínica hasta que haya mayor disponibilidad de datos8.
También DXA es imprecisa en adultos con patologías asociadas a baja talla, como las displasias esqueléticas, el síndrome de Turner, y el panhipopituitarismo, entre otros. Por otra parte, en patologías donde la proporción entre hueso trabecular y cortical está notoriamente alterada, DXA no aporta una evaluación útil. Este es el caso de los pacientes con insuficiencia renal, donde el hueso trabecular está aumentado y el cortical disminuido; así, en estos pacientes, DXA entrega una densitometría normal o alta, no aportando información precisa sobre el riesgo de fractura9,10.
Adicionalmente, en el campo de la investigación, es importante conocer en forma más completa los cambios propios de variables fisiológicas como el crecimiento o envejecimiento, como también, los que ocurren después de una intervención terapéutica. La obtención de información precisa sobre los compartimentos trabecular y cortical, así como sobre los cambios de la macroarquitectura, puede mejorar la comprensión de los resultados obtenidos.
Tomografía computada cuantitativa tridimensional
La tomografía computada cuantitativa axial de columna fue descrita al final de la década de los 70, y su uso se amplió en la de los 80. Con la aparición de DXA en 1988, el uso de QCT disminuyó. Sin embargo, el interés por esta técnica ha renacido debido a la importancia que tiene la arquitectura, la geometría ósea y la evaluación de una densitometría volumétrica real, especialmente útil en el campo de la investigación en osteología. La aparición de la tomografía computada helicoidal de multicorte, ha permitido el desarrollo de la tomografía computada cuantitativa tridimensional (QCT-3D). Esta técnica tiene como ventajas respecto al QCT convencional y la QCT bidimensional, un incremento significativo en la precisión del método (coeficiente de variación < 1%) y tiempos muy cortos de adquisición (< 1 min) lo que es importante en niños, al reducir los artefactos por movimiento. Por otra parte, comparado con QCT convencional, QCT-3D no requiere la optimización de la calidad de imagen, y por lo tanto la exposición a radiación puede ser reducida considerablemente4,5.
Descripción de la técnica QCT-3D
Como requerimientos materiales está el disponer de un scanner helicoidal, un fantoma con distintas concentraciones de hidroxiapatita sólida (habitualmente 0, 75, y 150 mg/cc), y un “software” o programa capaz de calcular las variable de densidad y geometría. Existen varias compañías comerciales que ofrecen estos productos, con ventajas variables de acuerdo a los objetivos de su uso4,5.
Tabla 1. Cuadro comparativo entre DXA y QCT.

En la evaluación de la columna, el paciente debe acostarse en decúbito dorsal en la tabla del scanner, con una almohada debajo de las rodillas para permitir su flexión relajada y lograr aplanamiento de la lordosis lumbar. Bajo la columna lumbar se debe ubicar el fantoma, y entre éste y la columna una bolsa plana de gel, para evitar artefactos debido al aire. En el caso del radio, el paciente debe acostarse en decúbito ventral con su brazo dominante estirado hacia adelante y la palma de la mano hacia abajo. Habitualmente se evalúan ambas tibias y el fantoma se pone bajo una de ellas (Figura 1 A).
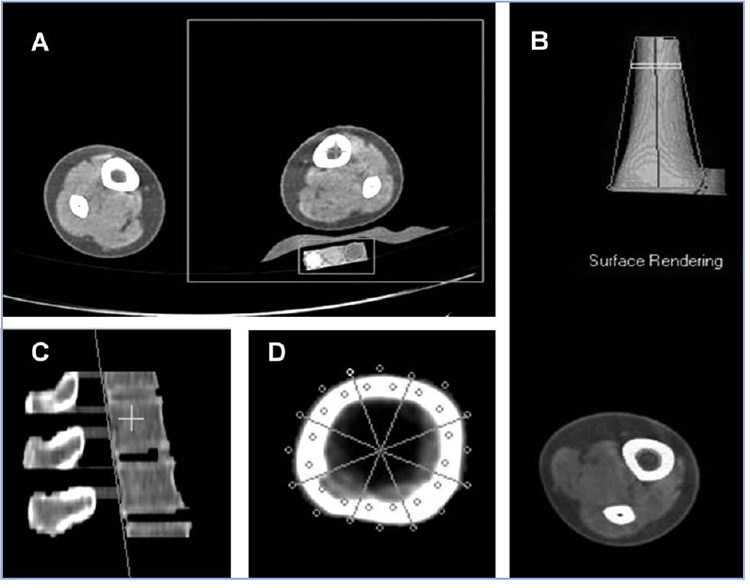
Figura 1. Parte superior: A: Sección del hueso a analizar es señalado con una cruz. El rectángulo menor muestra la detección, con posición correcta del fantoma, por el programa computacional. B: Reconstitución de la tibia seleccionada en A y selección del corte a analizar, señalado como rectángulo horizontal amarillo. Abajo selección de zona de hueso trabecular. Parte inferior: C: Separación de los cuerpos vertebrales de las apófisis espinosas (línea oblicua) y selección de la vértebra L2 (señalada por una cruz). D: Separación de los compartimentos trabecular y cortical en un corte de radio, con evaluación de los diámetros periosteal y endosteal y paracálculo de momento de inercia axial.
En la columna habitualmente se evalúan 4 vértebras de T12 a L3 o desde L1 a L4. En niños, para disminuir la exposición a la radiación, se escogen sólo 2, habitualmente L1 y L2. En el caso de las extremidades se pueden evaluar, radio, tibia y fémur; sin embargo, en función del interés clínico, los sitios mas usados son radio y tibia. Debido a la baja exposición radioactiva, comparada con la de columna, se pueden evaluar varias modalidades en el mismo hueso, que se identifican como 4, 50 y 65% del largo de la extremidad. En protocolos de investigación se evalúan aún más sitios: 4, 14, 20, 38, 66% de la longitud. En el caso de los niños es muy importante evitar el área de la placa de crecimiento, pues este sitio tiene una densidad mayor debido a la zona de calcificación provisoria4.
Una vez obtenidas las imágenes, estas son transferidas al programa, el cual calculará las variables deseadas y propias de cada sitio.
El sitio 4% de la tibia o del radio mide la densidad principalmente trabecular. En la zona de la diáfisis media, la densidad cortical. La zona de la diáfisis también es la escogida para evaluar variables geométricas como área ósea, grosor cortical, circunferencia periosteal y endosteal (Figura 1 D). En ella también se evalúan los parámetros dinámicos del hueso como el momento de inercia axial (AMI) y el índice de fuerza de tensión polar (SSI). AMI refleja la distribución del material óseo alrededor del centro del hueso, y SSI es una combinación del AMI mas la densitometría volumétrica de la corteza. Ambos índices están bien relacionados con el riesgo de fractura ósea4, 5.
Referencias
- Lewiecki EM, Gordon CM, Baim S, Leonard MB, Bishop NJ, Bianchi ML, et al. 2008. International Society for Clinical Densitometry 2007. Adult and Pediatric Official Positions. Bone. Aug 15 [Epub ahead of print].
- Seeman E. 2008. Bone quality: the material and structural basis of bone strength. J Bone Miner Metab; 26:1-8.
- Rauch F, Schonau E. 2001. Changes in bone density during childhood and adolescence: and approach based on bone’s biological organization. J Bone Miner Res;16:597-604.
- Ward K, Mughal Z, Adams J. 2007. Tools for measuring bone in children and adolescents. En: Bone Densitometry in growing patients. Guidelines for clinical practice. Editores: Sawyer AJ, Bachrach LK, Fung EB. Editorial, Humana Press; 15-40.
- A practical guide to bone densitometry in children. 2004. National Osteoporosis Society.
- Gordon CM, Bachrach LK, Carpenter TO, Crabtree N, El-Hajj Fuleihan G, et al. 2008. Dual energy X-ray absorptiometry interpretation and reporting in children and adolescents: the 2007 ISCD Pediatric Official Positions. J Clin Densitom 11: 43-58.
- Wren TA, Liu X, Pitukcheewanont P, Gilsanz V. 2005. Bone densitometry in pediatric populations: discrepancies in the diagnosis of osteoporosis by DXA and CT. J Pediatr 146: 776-779.
- Engelke K, Adams JE, Armbrecht G, Augat P, Bogado CE, Bouxsein ML, Felsenberg D, Ito M, Prevrhal S, Hans DB, Lewiecki EM.2008 Clinical use of quantitative computed tomography and peripheral quantitative computed tomography in the management of osteoporosis in adults: the 2007 ISCD Official Positions. J Clin Densitom 11 (1): 123-62.
- Bacchetta J, Boutroy S, Delmas P, Fouque D. 2008. Bone imaging in patient with chronic kidney disease: A new tool for managing renal osteodystrophy? Nephrol Ther. Aug 1. [Epub ahead of print] French.
- Leonard MB. 2007. A structural approach to the assessment of fracture risk in children and adolescents with chronic kidney disease. Pediatr Nephrol 22 (11): 1815-1824.