Efectos de la cirugía bariátrica sobre el metabolismo óseo
Juan P. Valderas I.1 y Gilberto González V.2
Effects of bariatric surgery on bone health
1Departamento de Nutrición, Diabetes y
Metabolismo.
2Departamento de Endocrinología. Facultad
de Medicina, Pontificia Universidad Católica
de Chile.
Correspondencia a:
Dr. Gilberto González V.
Departamento de Endocrinología
Facultad de Medicina
Pontificia Universidad Católica de Chile
Lira 85, piso 5
Santiago, Chile
Teléfono 56-2-354-3095
Fax 56-2-638-5675
E-mail: ggonzale@med.puc.cl
Recibido: 30 Noviembre de 2009
Aceptado: 14 Diciembre de 2009
There is concern about the long term complications of bariatric surgery and among these,
the derangements in bone metabolism that could increase the risk of osteopororosis. Most
studies show an elevated bone turnover in operated patients with loss of bone mass, that are
partially explained by the development of a secondary hyperparathyroidism. We have shown
that, among postmenopausal women, bone resorption remains elevated, even five years after
the operation, although not associated to loss of bone mass. The pathophysiology of these
alterations is complex and includes an reduction in mechanical load and calcium absorption
and postoperative changes in signaling hormones that have an effect on bone, coming
from adipose tissue (estrogens, leptin and adiponectin), liver (insulin like growth factor-1),
pancreas (insulin and amylin) or the bowel (ghrelin, glucagon-like peptide 2, peptide YY,
gastric inhibitory polypeptide). Available evidence suggest that bariatric surgery should be
considered a risk factor for osteoporosis. We recommend the incorporation of bone health in
pre operative evaluation. We also give suggestions to prevent the adverse effects of bariatric
surgery on bone health.
Key words: Bariatric surgery, Gastric bypass, Hyperparathyroidism, Bone, Obesity, Menopause.
La obesidad es una enfermedad de alta prevalencia que se asocia al desarrollo de diabetes mellitus, enfermedad cardiovascular, cáncer, dislipidemia, hipertensión arterial y otras patologías. Todo esto determina que el paciente obeso tenga aumento del riesgo de mortalidad y disminución en su expectativa de vida1. El tratamiento médico de la obesidad incluye dietas hipocalóricas, actividad física, terapia conductual y fármacos, intervenciones que producen pérdida de peso no muy acentuada y difícil de mantener en el tiempo2. Por otro lado, y principalmente en obesos mórbidos, la cirugía bariátrica o tratamiento quirúrgico de la obesidad, ha demostrado en el último tiempo alcanzar reducciones significativas de peso, con baja tasa de recidiva3 y asociada a disminución significativa de la morbimortalidad relacionada a la obesidad4-5. Esto ha generado un crecimiento explosivo de esta cirugía. De acuerdo a las encuestas de Buchwald et al en 36 países, en el año 2003 se efectuaron 146.301 cirugías bariátricas y en 2008 éstas alcanzaron a 344.2216-7. En nuestra institución, desde 1991 a la fecha se han realizado más de 4.000 cirugías bariátricas. Sin embargo, en el seguimiento a corto, mediano y largo plazo de pacientes sometidos a cirugía bariátrica se han descrito varios efectos secundarios de ésta, relacionados con alteraciones en la ingesta, absorción y metabolismo de varios macro y micronutrientes8. Derivado de esto, existe preocupación respecto a las posibles alteraciones que podría inducir la cirugía bariátrica en el metabolismo óseo y sus implicancias en el riesgo a largo plazo para el desarrollo de patologías óseas como osteoporosis u osteomalacia.
Este artículo revisa la evidencia disponible acerca de los efectos de la cirugía bariátrica sobre el metabolismo óseo, los mecanismos fisiopatológicos involucrados en ello y sugiere recomendaciones para prevenir el posible impacto negativo de éstos sobre la salud ósea.
El peso corporal como factor protector para osteoporosis y fracturas óseas
Numerosos estudios epidemiológicos han demostrado que existe una relación directa entre el peso corporal y la masa ósea, evaluada por la densidad mineral ósea o DMO. Más importante aún, se ha demostrado que existe una relación inversa entre el peso corporal y el riesgo de fracturas. Así, por ejemplo en el SOF (Study of Osteoporotic Fractures)9, se observó que el cuartil de mujeres más delgadas, mayores de 65 años, tenía el doble de riesgo relativo de presentar fracturas. En el meta-análisis de De Laet et al, que incluyó 12 cohortes con casi 60.000 hombres y mujeres, cada unidad de incremento del índice de masa corporal (IMC) se asoció a un 2% de disminución del riesgo de fracturas10. En otras cohortes, como las de Framingham11, Rancho Bernardo12, Oregon13 y la chino-americana14, el peso corporal explica entre un 10-20% de la DMO. En Chile, Lobo et al observaron, en una muestra de 166 mujeres de 15 a 55 años, correlación positiva entre el peso corporal y la DMO de columna y fémur de 0,33 y 0,26 respectivamente15.
Pérdida de peso, pérdida de masa ósea y
osteoporosis
El seguimiento en las cohortes de los estudios SOF, EPESE (Established Populations for the Epidemiologic Study of the Elderly)16 y NHANES I (National Health and Nutrition Examination Survey)17 mostró aumento del riesgo de fractura de 1,9-2,9 por cada 10% de pérdida de peso. Ramsdale et al18 y luego Compston et al19 fueron los primeros en observar que la baja de peso inducida por dieta hipocalórica, se asociaba a disminución de la DMO. Posteriormente, otros autores corroboraron estos hallazgos, de tal modo que la baja del 10% del peso implica disminución del 1 al 2% de la DMO. Estas publicaciones20-27 se resumen en la Tabla 1.
Es claro entonces que la obesidad se asocia a mayor DMO y menor riesgo de osteoporosis y fracturas. También que la pérdida del 10% de peso producto del tratamiento médico de la obesidad se acompaña de disminución del 1 al 2% de la DMO. Sin embargo, esta pérdida de peso, modesta en más del 90% de los sujetos, se recupera y no parece impactar significativamente la salud ósea. Algo muy distinto puede ocurrir en el tratamiento quirúrgico de la obesidad, donde se observan descensos de peso sostenidos que alcanzan 30 a 50% del peso previo.
Tabla 1. Efecto del tratamiento médico de la obesidad sobre la Densidad Mineral Ósea (DMO)
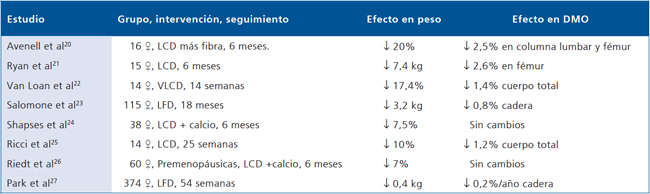 VLCD, dieta de muy bajas calorías (800-1000 cal); LCD, dieta de bajas calorías (1200-1500 cal); LFD, dieta baja en grasas. Referencias en texto.
VLCD, dieta de muy bajas calorías (800-1000 cal); LCD, dieta de bajas calorías (1200-1500 cal); LFD, dieta baja en grasas. Referencias en texto.
Metabolismo óseo en cirugía bariátrica
Desde la realización de los primeros procedimientos de la cirugía bariátrica en la década de los 50, se han utilizado gran variedad de técnicas. Muchas de éstas se han discontinuado, ya sea por su escaso éxito o por su inaceptable morbilidad.
En la actualidad, el Bypass gástrico en Y de Roux (BGYR), la Banda gástrica ajustable (BGA), la Gastrectomía vertical con banda y la Derivación bilio-digestiva con "switch" duodenal (DBP) son las técnicas más utilizadas. Además, una serie de otros procedimientos están actualmente en investigación y desarrollo, algunos de ellos en pacientes con obesidad moderada o sobrepeso, como Gastrectomía en manga y la Derivación doudeno-yeyunal.
El BGYR es la modalidad de cirugía más empleada actualmente en EE.UU., Chile y otros países6. Consiste en una técnica que combina un mecanismo restrictivo, creando una bolsa gástrica de 15 a 50 mL de capacidad, con un mecanismo malabsortivo, consistente en una derivación bilio-digestiva que deja un asa alimentaria de 50 a 150 cm. La BGA es otro procedimiento muy empleado en Australia, Europa y también en Chile6. Consiste en producir una bolsa gástrica de unos 30 mL a través de la instalación en la parte alta proximal del estómago de un dispositivo tipo brazalete conectado a un reservorio inflable emplazado en la pared abdominal que se emplea para ajustar la banda.
A pesar del gran incremento en la realización de estos procedimientos, los estudios del efecto de la cirugía bariátrica sobre el metabolismo óseo son escasos28-36 y se resumen en la Tabla 2. En general, estos estudios adolecen45 de importantes debilidades tales como, no ser controlados, tener tamaño muestral pequeño y corto seguimiento. A pesar de eso, la mayoría de ellos muestran pérdida significativa de DMO en los primeros 12 a 18 meses de la cirugía, periodo en que se produce la mayor baja de peso. La magnitud de disminución en la DMO es cercana a lo esperado para el grado de descenso de peso si se extrapola lo observado en los estudios sobre tratamiento médico. Esta pérdida de DMO se asocia habitualmente a incremento en marcadores de resorción ósea y a veces también en los de formación ósea. Estos cambios se observan principalmente en las cirugías con un componente malabsortivo o derivativo como el BGYR y la DBP. Sin embargo, al tener los individuos obesos, previamente a la cirugía, mayor masa ósea, el incremento de la resorción post cirugía no parece asociarse a aumento en la prevalencia de osteoporosis.
En lo que respecta a cambios del metabolismo cálcico, función paratiroidea o estado de vitamina D, la evidencia es más confusa. En los últimos años se ha descrito que los individuos obesos tienen mayor prevalencia de hipovitaminosis D37. Los mecanismos son variados e incluyen secuestro en el tejido adiposo de vitamina D, dado el carácter lipofílico de ésta, menor grado de exposición solar y menor síntesis a nivel cutáneo. Esto a veces se acompaña de niveles más altos de PTH, pero no de aumento de marcadores de resorción ósea38. La pérdida de peso posterior a la cirugía no se asocia necesariamente a disminución en los niveles de 25OHD, incluso en algunos estudios se observa un incremento, lo que podría deberse a liberación de depósitos de vitamina D desde el tejido adiposo. Por otro lado, algunos estudios muestran aumento de la PTH y de la prevalencia de hiperparatiroidismo secundario post BGYR y esto tendría directa relación con el grado de malabsorción intestinal determinado por el largo del asa alimentaria39.
A la fecha, no está claramente determinado en estudios prospectivos controlados si estos cambios del metabolismo óseo, incluyendo la pérdida de la DMO, se mantienen a largo plazo o se detienen en paralelo al descenso de peso. Nosotros demostramos en un estudio transversal, aumento en la resorción ósea en un grupo de 26 mujeres postmenopáusicas evaluadas 1 a 5 años post BGYR, comparadas con controles no operadas y pareadas por IMC (85% v/s 11% de valores elevados de carboxitelopéptido sérico o CTx). Además, en el grupo post BGYR el hiperparatiroidismo secundario fue 4 veces más frecuente comparado al control (35% v/s 8%), lo cual ocurrió independiente de la ingesta cálcica, estado de vitamina D o valores de ghrelina. A pesar de lo anterior no hubo diferencias en la DMO de ambos grupos, medida en columna lumbar y caderas. Nuestros resultados sugieren que en mujeres postmenopáusicas, grupo per se de mayor riesgo para osteoporosis, el BGYR incluso en el mediano plazo, se asocia a cambios negativos para la salud ósea, como resorción elevada e hiperparatiroidismo, pero que no determinan disminución de la DMO36. La importancia clínica de estos cambios en el metabolismo óseo en el largo plazo post BGYR no ha sido aún bien establecida.
Tabla 2. Efecto de la cirugía bariátrica sobre el metabolismo óseo
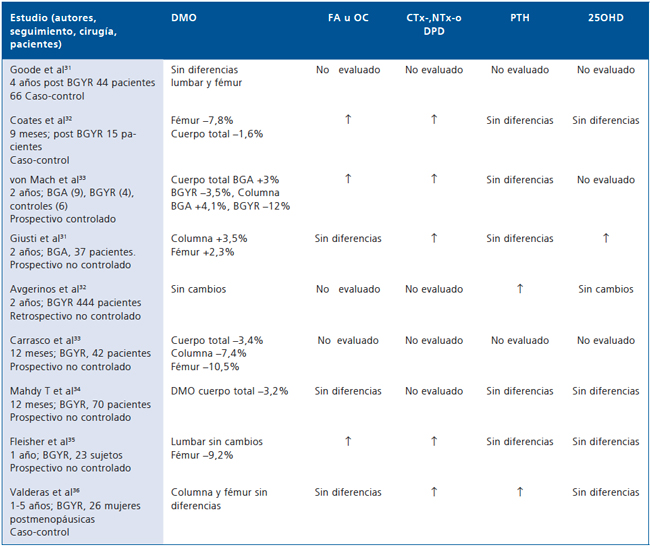
FA: Fosfatasas Alcalinas Totales; OC: Osteocalcina; CTx: Carboxitelopéptido; NTx: N-telopéptido;
DPD: deoxipiridolina. Referencias en texto.
DMO: Densidad Mineral Ósea.
Mecanismos fisiopatológicos
Tradicionalmente se ha establecido que el peso corporal y en especial la masa magra y la fuerza muscular, ejercen un efecto mecánico que estimula la formación de hueso por parte de los osteoblastos. Por otro lado, las pacientes obesas presentan mayores niveles plasmáticos de estrógenos y andrógenos, como testosterona, dehidroepiandrosteronasulfato y androstenediona, debido en parte al aumento de su producción en el tejido adiposo. Ambos tipos de esteroides sexuales, pero principalmente los estrógenos, suprimen la resorción ósea por su acción tanto directa como indirecta sobre los osteoclastos. Estos efectos protectores se perderían con la baja de peso40. También se ha postulado que los individuos que pierden peso tendrían menor ingesta de calcio. De hecho, la suplementación cálcica puede evitar la pérdida de DMO y el aumento en los marcadores de resorción41 en sujetos con pérdidas moderadas de peso producto de dietas hipocalóricas. La exclusión duodenal característica del BGYR y la DBP se asocia a malabsorción de calcio42, por la exclusión del duodeno y yeyuno alto, y probablemente también menor absorción y pérdida intestinal de vitamina D, debido a una pobre mezcla de sales biliares con el contenido intestinal y a la formación de sales insolubles6. Esto último, podría ser de mayor relevancia en grupos con alta prevalencia de hipovitaminosis D, como según nuestros estudios lo son las mujeres chilenas postmenopáusicas43; en tal contexto y con hiperparatiroidismo secundario frecuentemente asociado, la mal absorción de calcio posterior al BGYR podría empeorar el hiperparatiroidismo y llevar al desarrollo de hiperparatiroidismo terciario, como lo sugieren los hallazgos de nuestro estudio. Consecuente con esta hipótesis, uno de nosotros ha identificado en los últimos 2 años a dos pacientes con esta complicación post BGYR (GG, observaciones no publicadas).
En la fisiopatología de los cambios del metabolismo óseo post cirugía bariátrica, es importante considerar también, además de los esteroides sexuales, aquellos péptidos con acción sobre el metabolismo óseo y que son secretados normalmente desde el páncreas, hígado, tejido adiposo y tubo digestivo, los cuales pueden sufrir modificaciones post cirugía bariátrica. La insulina y el IGF-1 son reguladores del crecimiento de los osteoblastos que tienen receptores para ambas hormonas. La amilina, co-secretada con la insulina por las células beta pancreáticas, tendría la misma acción, además de producir un efecto símilar a la calcitonina sobre los osteoclastos. Todas estas hormonas están aumentadas en estados de resistencia a la insulina, como el que se observa en la obesidad, y disminuyen sus niveles con el descenso de peso44.
La leptina es una proteína secretada principalmente por el adipocito cuya concentración plasmática está directamente correlacionada con la cantidad de masa grasa. Las células de las líneas osteoblásticas expresan receptores para leptina, y su estimulación incrementa la diferenciación de los osteoblastos aumentando la mineralización de la matriz extracelular. Además, la leptina inhibe la expresión del RANK-L y aumenta la de osteoprotegerina (OPG). Estos hallazgos han sido confirmados en estudios intervencionales con modelos animales45. En humanos, algunos estudios han comunicado una asociación entre leptina y mayor DMO, menor riesgo de fracturas y disminución de la resorción ósea, pero otros investigadores han publicado resultados distintos46.
La adiponectina es la citoquina más abundante del plasma, producida por el tejido adiposo; sus niveles están reducidos en la obesidad y aumentan luego de la pérdida de peso. Se ha establecido que los osteoblastos humanos expresan adiponectina y sus receptores47 y que esta citoquina es capaz de estimular in vitro la proliferación y diferenciación de líneas celulares de osteoblastos. Sin embargo, dado la similitud estructural de la adiponectina con la familia del Factor de Necrosis Tumoral Alfa (entre los que está el RANK-L y la OPG) y a su capacidad de regular la acción del NFkappa beta, podría, por este mecanismo, estimular también la osteoclastogénesis48. Esto podría explicar la correlación negativa entre los niveles plasmáticos de adiponectina y la DMO, descrita por algunos autores en hombres y mujeres49. Carrasco et al, observaron una correlación positiva entre la disminución de la DMO y el incremento de adiponectina en pacientes sometidos a BGYR33.
La modificación anatómica del tubo digestivo también produce cambios en la secreción de una serie de péptidos intestinales, ya sea en períodos de ayuno o postprandiales. A la fecha se han descrito efectos sobre el metabolismo óseo para GIP (glucose-dependent insulinotropic peptide)50, PYY (péptido YY)51, GLP-2 (glucagon like peptide 2)52 y ghrelina53. La ghrelina, el primer ligando endógeno del receptor secretagogo de la hormona del crecimiento, fue descubierta por Kojima et al en 199954. El 75% es producido en el fondo gástrico, el resto en intestino delgado y sólo pequeñas cantidades por otros órganos. Ghrelina presenta niveles altos en periodos de ayuno, que disminuyen después de comer y su administración endovenosa tiene un potente efecto orexígeno en humanos y animales55. Hasta la fecha se han encontrado receptores para ghrelina en osteoblastos de ratas, pero aún no en los de humanos. In vitro, la ghrelina estimula la proliferación de osteoblastos humanos, pero no su diferenciación y en algunos estudios de cohorte, sus niveles plasmáticos en ayunas tienen una correlación positiva con DMO y negativa con marcadores de recambio óseo56. Un estudio en humanos no mostró que la administración endovenosa tuviera un efecto agudo sobre el metabolismo óseo57. Los cambios en los niveles plasmáticos de ghrelina varían según la modalidad de cirugía bariátrica. En los pacientes sometidos a BGA aumenta, en los que se hizo Gastrectomía en Manga disminuye y en los sometidos a BGYR, en que el remanente gástrico permanece dentro del abdomen, puede aumentar, mantenerse o disminuir58. En nuestro estudio las mujeres sometidas a BGYR tenían niveles en ayuno similares a los controles no operadas, pero el efecto protector sobre el hueso, expresado como correlación positiva con la DMO y negativa con PTH sólo fue observada en las mujeres sin BGYR36. La pérdida de este efecto positivo sobre el hueso de la ghrelina ha sido observado en otros situaciones patológicas: Misra et al en jóvenes anoréxicas comparadas con adolescente sanas59 y Hula et al, en sujetos gastrectomizados versus controles sanos57.
Recomendaciones
Evaluación pre-quirúrgica
Mientras no esté claramente establecido la significación del aumento en la resorción ósea y eventual pérdida de la DMO después de la cirugía la bariátrica, se debe considerar esta cirugía como un factor de riesgo para el desarrollo de osteoporosis; de hecho así lo incluyen las guías actualizadas de la National Osteoporosis Foundation de EE.UU.60 en el 2008. El impacto de este mayor riesgo para osteoporosis, podría ser más relevante en sujetos con riesgo ya aumentado, como mujeres postmenopáusicas, pacientes con fractura por fragilidad previa o aquellos con antecedente de fractura de cadera en padres, etc. En tales casos, es nuestra recomendación que se efectúe una evaluación completa de la salud ósea previa a la cirugía bariátrica, incluyendo junto al control médico especializado, exámenes como densitometría ósea de doble fotón radiológico (DXA) en columna lumbar, caderas y radio. Este último sitio es recomendado dado su mayor sensibilidad al exceso de PTH, y también por el hecho que en pacientes con peso mayor a 130 kg, la mesa del equipo de DXA habitualmente no permite realizar el estudio en los sitios clásicos. Además, esta evaluación debería incluir perfil bioquímico completo con calcemia, albuminemia y pruebas hepáticas, ya que los fosfatas alcalinas totales son un marcador adecuado de formación ósea si las pruebas hepáticas son normales61, PTH, 25OHD y calciuria de 24 horas. El objetivo de esta evaluación es precisar mejor el riesgo de osteoporosis, pesquisarla tempranamente si la hubiese y detectar si previamente a la cirugía bariátrica existen factores corregibles para así atenuar el impacto posterior en el metabolismo óseo, tales como baja ingesta cálcica, deficiencia de vitamina D o hiperparatiroidismo secundario. En tales casos, podría ser también de utilidad para el seguimiento la determinación de algún marcador de resorción ósea como deoxipiridolina urinaria o CTx. En pacientes con riesgo muy elevado de fractura osteoporótica, por ejemplo, fractura previa y/o DXA en nivel de osteoporosis, se debería evaluar el riesgo/beneficio global de la cirugía bariátrica o bien posponer ésta hasta haber iniciado tratamiento específico para disminuir el riesgo.
Manejo postoperatorio
Es bien conocido que en la población general la ingesta de calcio y vitamina D no alcanza los niveles adecuados y ello también se observa en los sujetos sometidos a cirugía bariátrica. De hecho, un punto aún no aclarado es cuál es la ingesta diaria recomendada de calcio y vitamina D en tales pacientes. Ya que se trata de pacientes con riesgo aumentado de osteoporosis y en el caso de BGYR y DBP con malabsorción per se, la ingesta adecuada de calcio y vitamina D, debería ser mayor a lo recomendado para sujetos similares sin cirugía bariátrica, es decir, 1.200 mg de calcio y 800 UI de vitamina D para los mayores de 50 años. Algunos estudios han demostrado que tal suplementación no basta para disminuir los niveles de los marcadores de resorción ni los de PTH. Carlin et al, estudió a 60 mujeres obesas mórbidas sometidas a BGYR con deficiencia de vitamina D, diagnosticada previamente a la cirugía y 30 de ellas fueron seleccionadas por azar para recibir 50.000 UI semanales adicionales de vitamina D. Luego de un año se observó, en el grupo de pacientes con suplementación adicional, corrección de la hipovitaminosis D en la mayoría de ellas, disminución en la pérdida de DMO en cadera y disminución en marcadores de resorción ósea comparados con el grupo con placebo y sin mayor incidencia de efectos adversos62. Mientras esperamos mayor evidencia es ya seguro suplementar a los pacientes post cirugía bariátrica con vitamina D hasta 2.000 UI/d. El tipo de suplemento de calcio utilizado para la suplementación también podría ser importante. Es sabido que la presencia de acidez gástrica es necesaria para la disolución de la mayoría de las sales de calcio, lo que afectaría más a las de carbonato o fosfato de calcio y menos al citrato. Recientemente, Tondapu et al, compararon el efecto del citrato de calcio versus el carbonato, y observaron que la ingesta de citrato resultaba en calcio sérico más alto y niveles de PTH más bajos63. Adicionalmente, el aporte de citrato podría aumentar la actividad inhibitoria en la orina respecto de la formación de cálculos, lo cual sería beneficioso en estos pacientes dado que también existe en ellos riesgo aumentado para nefrolitiasis64. Esto último se explicaría por la mayor incidencia de hiperoxaluria, bajo volumen urinario, aumento de la acidez urinaria e hipocitraturia, factores todos de riesgo para nefrolitiasis y consecuencia de la malabsorción digestiva65. Es recomendable para los pacientes post cirugía bariátrica, alcanzar ingesta cálcica de al menos 1.200 a 1.500 mg/d, de preferencia por dieta (lo que implica 4 porciones de lácteos/día) o en caso de suplementación farmacológica, de preferencia con sales de citrato de calcio en dosis fraccionadas de no más de 500 mg y controlando periódicamente valores de calciuria, citrato y PTH para ajuste de dosis.
Tratamiento de osteoporosis en pacientes post cirugía bariátrica.
Según nuestro mejor conocimiento, no se ha publicado hasta la fecha ningún estudio clínico sobre prevención o tratamiento de osteoporosis en sujetos sometidos a cirugía bariátrica. En este tipo de pacientes, portadores de cirugías con reducción del volumen gástrico y con o sin componente malabsortivo, es razonable dudar de la eficacia y seguridad del uso de la vía oral para suministrar los fármacos recomendados en la población general. Así, el uso de aquellos fármacos, disponibles para vía parenteral, como son Calcitonina en formulación nasal, Teriparatide de uso subcutáneo o bisfosfonatos de uso endovenoso como Ibandronato o Zoledronato, parecen muy promisorios para eventuales estudios en este tipo de sujetos o bien para el manejo específico de un paciente con osteoporosis post cirugía bariátrica.
Conclusiones
La creciente indicación de la cirugía bariátrica y sus potenciales efectos adversos sobre el metabolismo óseo, anticipan la ocurrencia cada vez más frecuente de pacientes con riesgo aumentado para su salud ósea derivado de la cirugía, o más aún con diagnóstico de osteoporosis y antecedente de cirugía bariátrica. Esta situación plantea múltiples desafíos en términos de conocer mejor la relación entre cirugía bariátrica, salud ósea y cómo manejar los pacientes en esta área. Como en otros casos, estos desafíos ofrecen una excelente oportunidad para el desarrollo de investigación multidisciplinaria innovadora, que deseamos sea próspera y fecunda en nuestro medio.
Referencias
- Fontaine KR, Redden DT, Wang C, Westfall AO, Allison DB. 2003. Years of life lost due to obesity. JAMA 289 (2): 187-193.
- Franz MJ, VanWormer JJ, Crain AL, Boucher JL, Histon T, Caplan W, et al. 2007. Weight-loss outcomes: a systematic review and meta-analysis of weight-loss clinical trials with a minimum 1-year follow-up. J Am Diet Assoc 107: 1755-1767.
- O'Brien PE, McPhail T, Chaston TB, et al. 2006. Systematic review of medium-term weight loss after bariatric operations. Obes Surg 16: 1032-1340.
- Adams TD, Gress RE, Smith SC, Halverson RC, Simper SC,
Rosamond WD et al 2007. Long-term mortality after gastric
bypass surgery. N Engl J Med 375: 753-761. - Buchwald H. Avidor Y, Braunwald E, Jensen MD, Pories W, Fahrbach K, et al. 2004. Bariatric surgery: a systematic review and meta-analysis. JAMA 292: 1724-1737. 30.
- Buchwald H, Williams S. Bariatric Surgery Worldwide. 2003. Obes Surg 2004 14: 1157-1164.
- Buchwald H, Oien DM. Metabolic/Bariatric Surgery worldwide. 2008. Obes Surg 2009 Noviembre 3 [en prensa].
- Bloomberg RD, Fleishman A, Nalle JE, Herron DM, Kini S. 2005. Nutritional deficiencies following bariatric surgery: what have we learned? Obes Surg 15: 145-154.
- Ensrud K, Lipschutz R, Cauley J, Seeley D, Nevitt M, Scott J, et al. 1997. Body size and hip fracture risk in older women: a prospective study. Am J Med 103: 274-280.
- De Laet C, Kanis JA, Odén A, Johanson H, Johnell O, Delmas P, et al. 2005. Body mass index as a predictor of fracture risk: a meta-analysis. Osteoporos Int 16: 1330-1338.
- Felson DT, Zhang Y, Hannan MT, Anderson JJ. 1993. Effects of weight and body mass index on bone mineral density in men and women: the Framingham study. J Bone Miner Res 8: 567-573.
- Edelstein SL, Barret-Connor E. 1993. Relation between body size and bone mineral density in elderly men and women. Am J Epidemiol 138: 160-169.
- Orwoll ES, Bevan L, Phipps KR. 2000. Determinants of bone mineral density in older men. Osteoporos Int 11: 815-821.
- Walker MD, Babbar R, Opotowsky A, McMahon DJ, Bilezikian JP. 2007. Determinats of bone mineral density in Chinese-American women. Osteopros Int 18: 471-478.
- Lobo G, Ladrón de Guevara D, Zerboni A. 2004. Densitometría ósea en mujeres chilenas en edad fértil: correlación con valores referenciales y variables antropométricas. Rev Méd Chile 132: 681-690.
- Langlois JA, Harris T, Looker AC, Madans J. 1996. Weight change between age 50 years and old age is associated with risk of hip fracture in white women aged 67 years and older. Arch Intern Med 156: 989-994. 16.
- Langlois JA, Mussolino ME, Visser M, Looker AC, Harris T, Madans J. 2001. Weight loss from maximum body weight among middle-aged and older white women and the risk of hip fracture: the NHANES I epidemiologic follow-up study. Osteoporos Int 12: 763-768.
- Ramsdale SJ, Bassey EJ. 1994. Changes in bone mineral density associated with dietary-induced loss of body mass in young women. Clin Sci (Lond) 87: 343-348.
- Compston JE, Laskey MA, Croucher PI, Coxon A, Kreitzman S. 1992. Effect of diet-induced weight loss on total body bone mass. Clin Sci (Lond) 82: 429-432.
- Avenell A, Richmond PR, Lean ME, Reid DM. 1994. Bone loss associated with a high fibre weight reduction diet in postmenopausal women. Eur J Clin Nutr 48: 561-566.
- Ryan AS, Nicklas BJ, Dennis KE. 1998. Aerobic exercise maintains regional bone mineral density during weight loss in postmenopausal women. J Appl Physiol 84: 1305-1310.
- Van Loan MD, Johnson HL, Barbieri TF. 1998. Effect of weight loss on bone mineral content and bone mineral density in obese women. Am J Clin Nutr 67: 734-738.
- Salamone LM, Cauley JA, Black DM, Simkin-Silverman L, Lang W, Gregg E, et al. 1999. Effect of a lifestyle intervention on bone mineral density in premenopausal women: a randomized trial. . Am J Clin Nutr 70: 97-103.
- Shapses SA, von Thun NL, Heymsfield SB, Ricci TA, Ospina M, Pierson RN et al. 2001. Bone turnover and density in obese premenopausal women during moderate weight loss and calcium supplementation. J Bone Miner Res 16: 1329-1336. 1.
- Ricci TA, Heymsfield SB, Pierson RN Jr, Stahl T, Chowdhury HA, Shapses SA. 2001. Moderate energy restriction increases bone resorption in obese postmenopausal women. Am J Clin Nutr 73: 347-352.
- Riedt C, Schlussel Y, von Thun N, Ambia-Sobhan H, Stahl T, Field M, et al. 2007. Premenopausal overweight women do not lose bone during moderate weight loss with adequate or higuer calcium intake. Am J Clin Nutr 85: 972-980.
- Park HA, Lee JS, Kuller LH, Cauley JA. 2007. Effects of weight control during the menopausal transition on bone mineral density. J Clin Endocrinol Metab 92: 3809-3815.
- Coates PS, Fernstrom JD, Fernstrom MH, Schauer PR, Greenspan SL. 2004. Gastric bypass surgery for morbid obesity leads to an increase in bone turnover and a decrease in bone mass. J Clin Endocrinol Metab 89: 1061-1065.
- Goode LR, Brolin RE, Chowdhury HA, Shapses SA. 2004. Bone and gastric bypass surgery: effects of dietary calcium and vitamin D. Obes Res 12: 40-47.
- von Mach MA, Stoeckli R, Bilz S, Kraenzlin M, Langer I,
Keller U. 2004. Changes in bone mineral content after surgical
treatment of morbid obesity. Metabolism 53: 918-921. - Giusti V, Gasteyger C, Suter M, Heraief E, Gaillard RC, Burckhardt. 2005. Gastric banding induces negative bone remodelling in the absence of secondary hyperparathyroidism: potential role of serum C telopeptides for follow-up. Int J Obes (Lond) 29: 1429-1435.
- Avgerinos DV, Leitman IM, Martínez RE, Liao EP. 2007. Evaluation of markers for calcium in a population of obese adults undergoing gastric bypass operations. J Am Coll Surg 205: 294-297.
- Carrasco F, Ruz M, Rojas P, Csendes A, Rebolledo A, Codoceo J, et al. 2009. Changes in bone mineral density, body composition and adiponectin levels in morbidly obese patients after bariatric surgery. Obes Surg 19: 41-46.
- Mahdy T, Atia S, Farid M, Adulatif A. 2008. Effect of Roux-en Y gastric bypass on bone metabolism in patients with morbid obesity: Mansoura experiences. Obes Surg 18: 1526-531.
- Fleischer J, Stein EM, Bessler M, Della Badia M, Restuccia N, Olivero-Rivera L, et al. 2008. The decline in hip bone density after gastric bypass surgery is associated with extent of weight loss. J Clin Endocrinol Metab 93: 3735-3740.
- Valderas JP, Velasco S, Solari S, Liberona Y, Viviani P, Maiz A, et al. 2009. Increase of bone resorption and the parathyroid hormone in postmenopausal women in the long-term after Roux-en-Y Gastric Bypass. Obes Surg 19: 1132-1138.
- Goldner WS, Stoner JA, Thompson J, Taylor K, Larson L, Erickson J, et al. 2008. Prevalence of vitamin D insufficiency and deficiency in morbidly obese patients: a comparison with nonobese controls. Obes Surg 18: 145-150.
- Rueda S, Fernández-Fernández C, Romero F, Martínez de Osaba J, Vidal J. 2008. Vitamin D, PTH, and metabolic syndrome in severely obese subjects. Obes Surg 18: 151-154.
- Johnson JM, Maher JW, DeMaria EJ Downs RW, Wolfe LG, Kellum JM. 2006. The long-term effects of gastric bypass on vitamin D metabolism. Ann Surg 243: 701-704.
- Wardlaw G. 1996. Putting body weight and osteoporosis into perspective. Am J Clin Nutr 63 (suppl): 433S-436S.
- Radak TL. 2004. Caloric restriction and calcium'effect on bone metabolism and body composition in overweight and obese premenopausal women. Nutr Rev 62: 468-481.
- Riedt CS, Brolin RE, Sherrel RM, Field MP, Shapses SA. 2006. True fractional calcium absorption is decreased after Roux-en-Y gastric bypass surgery. Obesity 14: 1940-1948.
- González G, Alvarado JN, Rojas A, Navarrete C, Velásquez C, Arteaga E. 2007. High prevalence of vitamin D deficiency in Chilean healthy postmenopausal women with normal sun exposure: additional evidence for a worldwide concern. Menopause 14: 455- 461.
- Reid IR. 2008. Relationships between fat and bone Osteoporos Int 19: 595-606
- Thomas T. 2004. The complex effects of leptin on bone metabolism through multiple pathways. Curr Opin Pharmacol 4: 295-300.
- Weiss LA, Barret-Connor E, von Muhlen D, Clark P. 2006. Leptin Predicts BMD and Bone Resorption in Older Women but Not Older Men: The Rancho Bernardo Study. J Bone Miner Res 21: 758-764. 46.
- Berner HS, Lyngstadaas SP, Spahr A, Monjo M, Thommesen L, Drevon CA. 2004. Adiponectin and its receptors are expressed in bone-forming cells. Bone 35: 842-849.
- Luo XH, Guo LJ, Yuan LQ, Xie H, Zhou HD, Wu XP. 2005.
Adiponectin stimulates human osteoblasts proliferation and
differentiation via the MAPK signaling pathway. Exp Cell Res; 309 (1): 99-109. - Lenchik L, Register TC, Hsu FC, Lohman K, Nicklas BJ, Freedman BI, et al. 2003. Adiponectin as a novel determinant of bone mineral density and visceral fat. Bone 33: 646-651.
- Ding KH, Shi XM, Zhong O, Kang B, Xie D, Bollag WB, et al. 2008. Impact of Glucose –Dependent Insulinotropic Peptide on Age-Induced Bone Loss 2. J Bone Miner Res 23: 870-878.
- Wortley KE, García K, Okamoto H, Thabet K, Anderson KD, Shen V et al. 2007. Peptide YY regulates bone turnover in rodents. Gastroenterology 133: 1534-1543.
- Henriksen DB, Alexandersen P, Bjarnson NH, Vilsboll T,
Hartmann B, Henriksen EE et al. 2003. Role of gastrointestinal
hormones in postprandial reduction of bone resorption. J Bone Miner Res 18: 2180-2189. - van der Velde M, Delhanty P, van der Eerden B, van der Lely AJ, van Leeuwen J. 2008. Ghrelin and bone. Vitam Horm 77: 239-258.
- Kojima M, Hosoda H, Date Y, Nakazato M, Maysuo H, Kangawa K. 1999. Ghrelin is a growth-hormone-releasing acylated peptide fron stomach. Nature 402: 656-660.
- Leite-Moreira AF, Soares JB. 2007. Physiological, pathological and potential therapeutic roles of ghrelin. Drugs Discov Today 12: 276-288.
- Weiss LA, Langenberg C, Barrett-Connor E. 2006. Ghrelin and bone: is there an association in older adults?: the Rancho Bernardo study. J Bone Miner Res 21: 752-757.
- Huda MS, Durham BH, Wong SP, Dovey TM, McCulloch P, Kerrigan D et al. 2007. Lack of an acute effect of ghrelina on markers of bone turnover in healthy controls and post-gastrectomy subjects. Bone 41: 406-413.
- Langer FB, Reza Hoda MA, Bohdjalian A, Felberbauer FX, Zacherl J, Wenzl E, et al. 2005. Sleeve gastrectomy and gastric banding: effects on plasma ghrelin levels. Obes Surg 15: 1024- 1029.
- Misra M, Miller KK, Stewart V, Hunter E, Kuo K, Herzog DB, Klibanski A. 2005. Ghrelin and bone metabolism in adolescent girls with anorexia nervosa and healthy adolescents. J Clin Endocrinol Metab 90: 5082-5087.
- http://www.nof.org/professionals/NOF_Clinicians_Guide.pdf
- Woitge HW, Seibel MJ, Ziegler R. 1996. Comparison of total and bone-specific alkaline phosphatase in patients with nonskeletal disorder or metabolic bone diseases. Clin Chem 42: 1796-1804.
- Carlin AM, Rao DS, Yager KM, Parikh NJ, Kapke A. 2009. Treatment of vitamin D depletion after Roux-en-Y gastric bypass: a randomized prospective clinical trial. Surg Obes Relat Dis 5: 444-449.
- Tondapu P, Provost D, Adams-Huet B Sims T, Chang C, Sakhaee K. 2009. Comparison of the absorption of calcium carbonate and calcium citrate after Roux-en-Y gastric bypass. Obes Surg 19: 1256-1261.
- Whitson JM, Stackhouse GB, Stoller ML. 2009. Hyperoxaluria after modern bariatric surgery: case series and literature review. Int Urol Nephrol. Jul 2. [Epub ahead of print].
- Park AM, Storm DW, Fulmer BR Still CD, Wood GC, Hartle JE 2nd. 2009. A prospective study of risk factors for nephrolithiasis after Roux-en-Y gastric bypass surgery. J Urol 182: 2334-2339.