Insulina degludec en pacientes diabéticos tipo 1. Observación a 18 meses
Lilian Sanhueza1,2, Pilar Durruty1,3,a, Elizabeth Toro1,b, Daniel Moreno4, Manuel García de los Ríos1
Degludec insulin in type 1 diabetic patients: 18 months of observation
1.Unidad de Diabetes, Hospital San Juan de Dios, Departamento de Medicina, Servicio de Salud Metropolitano Occidente
2. Facultad de Medicina, Universidad de Santiago de Chile
3. Sección de Endocrinología y Diabetes, Hospital Clínico Universidad de Chile
4. Residente de Cirugía Pontificia Universidad Católica de Chile
a. Bioquímico
b. Enfermera
No hubo aporte financiero
Correspondencia:
Lilian Sanhueza
Dirección: Fray Camilo Henríquez 175 Depto.
404 Santiago
Teléfono celular: +569 85951069
Correo electrónico: lilianllay@yahoo.es
Recibido: 30-08-2018
Aceptado: 07-11-2018
Resumen: Antecedentes: En el tratamiento de la diabetes se buscan insulinas de acción más prolongada y con menores tasas de hipoglicemias. Objetivo. Uso del análogo de insulina de acción ultralenta degludec en diabéticos tipo 1 (DM1) tratados previamente con glargina. Pacientes y método: Se observaron 230 DM1 durante 18 meses, promedio de edad 34 años y de diagnóstico 14 años, registrándose parámetros clínicos, bioquímicos, hipoglicemias y requerimientos de insulina (U/kg/peso), en régimen basal/bolo, con degludec y ultra-rápida precomidas. Degludec se ajustó quincenalmente. Resultados: A los 3 meses, la glicemia de ayunas disminuyó de 253mg/dl (243-270) a 180 mg/dl (172- 240), (p< 0,05); a los 6 meses a 156 mg/dl (137-180) (p< 0,05), a los 12 meses a 151 mg/dl (50-328) (p< 0,001) y a los 18 meses 150 (50-321) (p<0,001). La HbA1c, inicialmente de 10,6% (10,3-12,2) bajó a los 3 meses a 8,7% (8,2-11,1) (p< 0,05), a 6 meses a 8,3% (8,0-9,6) (p<0,05), a los 12 meses subió 9,0% (5,9-14,5) (p<0,001) y a los 18 meses 9,0% (5,9-14,6) (p<0,001). La dosis de degludec fue 0,5 U/kg/peso a los 18 meses. Hubo reducción de hipoglicemias: a los 3 meses 14 leves, 4 moderados 1 grave; a los 6 meses 8 leves, 2 moderados y ninguna grave; a los 12 meses 1 leve, y a los 18 meses 2 leves, 1 moderado y ninguna grave. Un 7,8% no presentó hipoglicemias. Conclusión: Degludec en DM1 mostró reducir las glicemias de ayunas y HbA1c, y menor número de hipoglicemias.
Palabras clave: Diabéticos tipo 1; Insulina glargina; Insulina degludec.
Abstract: Background: In the treatment of diabetes, longer-acting insulins with lower rates of hypoglycaemia are sought. Objective. Use of ultralow-acting insulin analog degludec in type 1 diabetic patients (T1D) previously treated with glargine. Patients and method: 230 T1D patients were observed during 18 months, average of age 34 years and of diagnosis 14 years, registering clinical, biochemical, hypoglycemia and insulin requirements (U / kg / weight), in basal / bolus regimen, with degludec and ultra-fast pre-meals. Degludec adjusted himself fortnightly. Results: At 3 months, the fasting glycemia decreased from 253 mg / dl (243-270) to 180 mg / dl (172 - 240), (p <0.05); at 6 months at 156 mg / dl (137-180) (p <0.05), at 12 months at 151 mg / dl (50-328) (p <0.001) and at 18 months 150 (50-321) ;(p <0.001). HbA1c, initially of 10.6% (10.3-12.2), decreased after 3 months to 8.7% (8.2 - 11.1) (p <0.05), to 6 months to 8 months, 3% (8.0-9.6) (p <0.05), at 12 months it rose 9.0% (5.9-14.5) (p <0.001) and at 18 months 9.0 % (5.9-14.6) (p <0.001). The dose of degludec was 0.5 U / kg / weight at 18 months. There was reduction of hypoglycemia: at 3 months, 14 mild, 4 moderate, 1 severe; at 6 months 8 mild, 2 moderate and none serious; at 12 months 1 mild, and at 18 months 2 mild, 1 moderate and none serious. 7.8% did not present hypoglycemia. Conclusion: Degludec in T1D patients showed to reduce fasting glycemia and HbA1c, and lower number of hypoglycemia.
Keywords: Insulin degludec; Insulin glargine; Type 1 diabetes.
Introducción
Los análogos de insulina, incorporados desde hace algunos años en el manejo de la diabetes1,2,3, presentan beneficios en el control metabólico y reducción de las hipoglicemias. Es un hecho conocido que cuanto más estricto es el control glicémico, mayor es la frecuencia de hipoglicemias, tanto en diabéticos tipo 1 (DM1) como en tipo 2 (DM2).
La insulina degludec (IDeg), análogo de acción ultraprolongada, es el resultado de cambios realizados a la molécula de insulina humana: remoción del aminoácido (aa) treonina en posición B30 y adición al aa lisina en posición 29 de un ácido graso de 16 carbonos, por medio del ácido glutámico4. Esta modificación confiere a la IDeg propiedades que le permiten formar un depósito soluble de multi-hexámeros tras su administración subcutánea. Se produce una liberación paulatina de iones de zinc y una disociación gradual de los monómeros de insulina, que pasan a la circulación de forma lenta y sostenida. Su perfil farmacocinético es plano y estable, su vida media es de aproximadamente 25 h y tiene una menor variabilidad glicémica reducida respecto a otros análogos de acción lenta5,6.
Nosotros publicamos un trabajo de eficacia y seguridad de la IDeg comparada con insulina glargina (IGlar) en DM1, encontrando a los 6 meses de tratamiento reducción de la glicemia de ayunas, de la HbA1c y menor tasa de hipoglicemia7. Birkeland en un estudio multicéntrico con una inyección diaria de IDeg y el agregado de insulina aspártica ultrarrápida en bolos precomidas; los autores concluyen que la IDeg tiene una eficacia similar a la IGlar, pero con menor frecuencia de hipoglicemias8. A igual conclusión llegó Dzygalo, además agregó que el uso de IDeg se asoció a menores requerimientos de insulina9.
Pacientes y método
Se ingresaron 230 DM1, 120 hombres y 110 mujeres, seguidos durante 18 meses, edad promedio 34 años (rango 15-58), antigüedad de la diabetes 14 años (3-46), en control en la Unidad de Diabetes del Hospital San Juan de Dios, Santiago. Todos firmaron el consentimiento informado para el cambio de la insulina. Los pacientes estaban en tratamiento con IGlar (U-100) en dos dosis al día como insulina basal y bolos de ultrarrápida precomidas a dosis fija, y ajustes de acuerdo a los requerimientos, a la sensibilidad preestablecida de cada individuo y al conteo de carbohidratos. Los pacientes tenían HbA1c superior a 10%.
Los DM1 cambiados a IDeg presentaban comorbilidades, tales como: cardiopatía coronaria 30%, nefropatía diabética 35%, hipertrigliceridemia 53% e hipertensión arterial 45%. Dos sujetos estaban en hemodiálisis trisemanal y dos eran trasplantados renales.
La IGlar se cambió por IDeg, iniciándose esta última con 0,3 U/kg/peso y ajustes quincenales, según los registros individuales de tres glicemias capilares al día realizadas por los pacientes en ayunas, prealmuerzo y precena. La IDeg se inyectó en una dosis diaria matinal respetando un horario fijo. La insulina ultrarrápida se mantuvo al inicio igual que la empleada cuando usaban IGlar. Los controles por enfermería se realizaron cada 15 días y mensualmente con nutricionista.
Los DM1 fueron evaluados a los 3, 6, 12 y 18 meses de iniciada nueva terapia; el 95% de los pacientes asistió a todos los controles. Se consideraron los siguientes parámetros: índice de masa corporal (IMC kg/m2), presión arterial sistólica y diastólica (mm Hg), colesterol total (mg/dl), colesterol HDL (col-HDL) (mg/dl), colesterol LDL (col-LDL) (mg/dl), triglicéridos (TG) (mg/dl), creatinina (mg/dl) y las variaciones de las dosis de insulina (U/kg/peso). Las glicemias, el col-HDL y los TG se midieron con métodos enzimáticos colorimétricos en un equipo automatizado Architec 8.000, con coeficientes de variación (CV) <5%. Para las glicemias se usó hexoquinasa/6, para el col-HDL y TG un detergente acelerador selectivo. Las HbA1c se determinaron en columnas de cromatografía líquida de alta resolución (HPLC) con un CV <5%, utilizando un equipo HPLC Variant 2000. La presión arterial se tomó en cada visita, repetida y con un esfigmomanómetro de Hg, estando los pacientes sentados y sin haber fumado ni recibido alimentos recientemente. El peso y la talla se midieron en una balanza marca Seca con cartabón. El IMC como peso/talla2 (kg/m2).
Respecto a las hipoglicemias, definidas como glicemia capilar <70 mg/dl), los episodios se registraron como diurnos y nocturnos. El grado de severidad se calificó como leve, moderado y grave, considerándose leve aquella sin compromiso neurológico y manejada por el propio paciente; moderada cuando presentaba alteración de conciencia, pero la persona tenía un estado de alerta suficiente, como para tratarla por sí misma y grave cuando necesitó la atención de terceros.
Las variables clínicas, antropométricas y de laboratorio se expresaron como promedio y rango. A los pacientes se les citó cada 15 días para revisión de los registros de glicemias capilares y vigilancia de eventuales hipoglicemias, con reeducación constante en el manejo de éstas.
Análisis estadístico: de normalidad con Shapiro-Wilk y pruebas de ANOVA (distribución normal) y Kruskal Wallis (no normal); nivel de significancia p<0,05.
Resultados
Los DM1 tenían con IGlar (al inicio del tratamiento con IDeg) glicemias de ayunas de 253 mg/dl (243-270), las que disminuyeron a los 3 meses de terapia con IDeg a 180 mg/dl (172-240), descendieron a 156 mg/dl (137-180) a los 6 meses, 151 mg/dl (50-328) a los 12 meses y 150 mg/dl (50-321) a los 18 meses (p<0,05) (Figura 1).
En relación a los niveles de HbA1c se observó un comportamiento similar al de las glicemias de ayunas; el valor basal (con IGlar) fue de 10,6% (10,3-12,2), a los 3 meses bajó a 8,7% (8,2-11,1), a los 6 meses a 8,3% (8,0-9,6), a los 12 meses subió a 9,0% (5,9-14,5) y a los 18 meses se mantuvo en 9,0% (5,9-14,6) (p<0,05) (Figura 2).
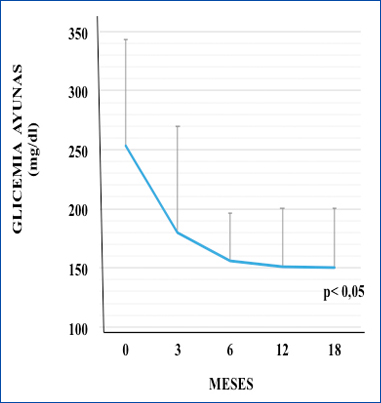 Figura 1. Pacientes diabéticos tipo 1 en tratamiento con insulina degludec.
Glicemias de ayunas a los 0, 3, 6, 12 y 18 meses de seguimiento
Figura 1. Pacientes diabéticos tipo 1 en tratamiento con insulina degludec.
Glicemias de ayunas a los 0, 3, 6, 12 y 18 meses de seguimiento 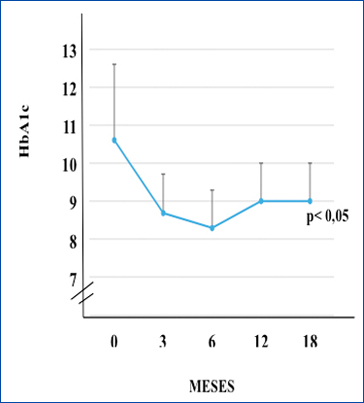 Figura 2. Pacientes diabéticos tipo 1 en tratamiento con insulina degludec.
HbA1c a los 0, 3, 6, 12 y 18 meses de seguimiento.
Figura 2. Pacientes diabéticos tipo 1 en tratamiento con insulina degludec.
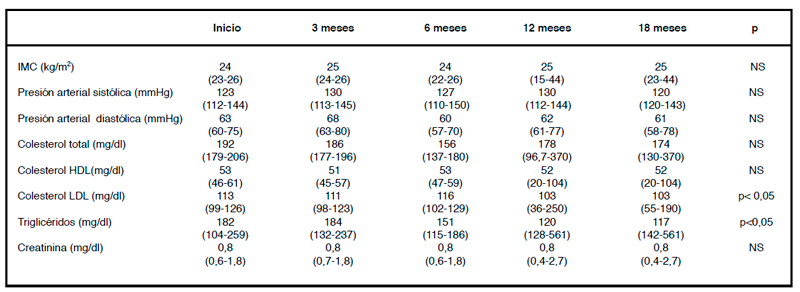
HbA1c a los 0, 3, 6, 12 y 18 meses de seguimiento. En la tabla 1 se presentan las características antropométricas, clínicas y metabólicas de los 230 casos. Se aprecia que no hubo cambios en el promedio de IMC en toda la observación (NS); aunque hubo casos que aumentaron de peso. No se registraron modificaciones en la presión arterial. El colesterol total, col-HDL, presión arterial sistólica y diastólica y la creatinina no se modificaron (NS). Los TG bajaron en promedio de 182 a 117 mg/dl (p< 0,05) y el col-LDL de 113 a 103 mg/dl (p< 0,05).
Tabla 1. Características antropométricas, clínicas y metabólicas de los pacientes DM1 al inicio 3, 6, 12 y 18 meses de seguimiento.
La dosis de IGlar administrada a los pacientes antes de cambiar a IDeg era de 0,7 U/kg/peso (0,6-0,8); el tratamiento con esta última se inició con 0,3 U/kg/peso, dosis que se mantuvo a los tres meses, subió a los seis a 0,4 y se estabilizó en 0,5 U/kg/peso a los 12 meses de terapia.
No hubo manifestaciones de lipodistrofia, ni alergia en el sitio de punción.
En relación a las hipoglicemias, durante los tres primeros meses de tratamiento se registró un promedio mensual de 19 eventos: 14 leves, 4 moderadas y una grave, a los seis se presentaron 8 leves y 2 moderadas y ninguna grave; a los 12 una sola leve y ninguna moderada ni grave. A los 18 meses, dos leves una moderada y ninguna grave. Hipoglicemias nocturnas se registraron sólo en 4 pacientes (1,7%).
Desde iniciada la IDeg, 70 pacientes (30%) no presentaron hipoglicemias.
Discusión
La fortaleza de nuestro estudio reside en el número de pacientes incluidos (230 casos) y una observación prolongada a 18 meses. El Clinical Trial Switch 1 tiene una muestra mayor y más tiempo de seguimiento10; en otras publicaciones las dos condiciones eran menores7,11,12,13.
En esta investigación no se descarta la posibilidad de sesgo por la vigilancia y seguimiento muy estrecho de los pacientes. Además, la edad de los DM1 fluctuaban en un rango muy amplio, 18 a 58 años, con motivaciones y situaciones metabólicas diferentes, hecho que puede haber influido en los resultados.
El estudio BEGIN12 en 52 semanas de duración, demostró que IDeg no fue superior a la IGlar en la reducción de las glicemias de ayunas, ni en la HbA1c; resultados diferentes a los obtenidos por nosotros, que observamos una reducción de la glicemia de ayunas y HbA1c a partir de los 3 meses, que se mantuvo constante hasta el final de la observación.
En nuestro análisis, en relación a las dosis de insulina, ellas se mantuvieron en 0,5 U/kg peso a los 12 meses, levemente más bajas que lo informado por Nakae13, quien encontró que éstas disminuyeron de 0,71 U/kg peso a 0,67 (p<0,02) a los 6 meses del uso de IDeg. Dzygalo, en un metaanálisis, también confirmó la reducción de la dosis de insulina comparado con otros análogos ultralentos9. Yamamoto refiere que el requerimiento de insulina al usar IDeg se redujo en un 25%, pero que la variabilidad glicémica en 24 horas no fue diferente a IGlar5. El autor concluye que las dos dosis de esta última pueden ser reemplazadas por una inyección de IDeg. Hallazgos que concuerdan plenamente con lo publicado por casi todos los autores8,9,13,14,15.
El apoyo de enfermería, contribuyó a una mejoría del control glicémico al lograr una mayor estabilidad emocional. Estos resultados son concordantes con lo informado por otros autores14,15.
Respecto a las hipoglicemias y contrariamente a lo informado por Nakae13 quien no observó diferencias en cuanto a frecuencia y severidad de éstas al comparar con IGlar; nuestro estudio mostró una reducción de las hipoglicemias durante los 18 meses de observación, desaparición de las hipoglicemias graves desde los 6 meses y menor número de episodios moderados y leves. Otras investigaciones sobre el uso clínico de IDeg concluyen que esta insulina minimiza el riesgo de hipoglicemias nocturnas2,17,18,19.
Koehler estudió la respuesta fisiológica aguda frente a una hipoglicemia inducida por IDeg e IGlar, no se registró diferencias en los síntomas ni en la función cognitiva; sin embargo los pacientes con IDeg tenían niveles moderadamente superiores de hormona de crecimiento, cortisol, adrenalina y noradrenalina, pero similares en glucagón, frente a iguales tiempos de recuperación de las glicemias16.
Otras publicaciones con IDeg informan una reducción de los días-cama de internación, lo que además de ser muy favorable para el paciente se traduce en ahorro en costos hospitalarios20,21,22.
Podemos concluir que la insulina IDeg en DM1 comparada con IGlar, muestra una glicemias de ayunas y de HbA1c más bajas, un efecto metabólico que cubre las 24 h; así como un menor riesgo de hipoglicemias.
Referencias
- Simó R. Nueva insulina basal de acción ultralenta: insulina degludec. Av Diabetol 2013; 29: 4-11.
- Muñoz M. Degludec, una nueva insulina basal de acción ultra-lenta para el tratamiento de la diabetes tipo 1 y 2: avances en investigación clínica. Endocrin Nutr 2014; 61: 153-159.
- Vora J, Cariou B, Evans M, Gross JL, Harris S, Landstedt-Hallin L, et al. Clinical use of insulin degludec. Diabetes Res and Clin Pract 2015; 109: 19-31.
- Berard L, MacNeill G. Insulin degludec, a long-acting-daily basal analogue for type 1 and type 2 diabetes mellitus. Can J Diabetes 2015; 39: 4-9.
- Yamamoto C, Miyoshi, Fujiwara Y, Kaneda R, Ichiyama M, Nomoto H. Degludec is superior to glargine in terms of daily glycemic variability in people with type 1 diabetes mellitus. Endocrin J 2016; 63: 53-60.
- Heise T, Korsatko S, Nosek L, Coester HV, Deller S, Roepstorff C, et al. Steady state is reached within 2-3 days of once-daily administration of degludec, a basal insulin with an ultralong duration of action. Diabetes 2016; 8: 132-138.
- Sanhueza L, Durruty P, Santibañez G, Toro E, Miranda JP, García de los Ríos M. Experiencia con insulina degludec en pacientes diabéticos tipo 1 del Hospital San Juan de Dios, Santiago, Chile. Rev Chil Endocrinol 2017; 10: 131-136.
- Birkeland KI, Home PD, Wendish U, Ratner KE, Johansen T, Endahl L, et al. Insulin degludec in type 1 diabetes: a randomized controlled trial of a new-generation ultra-long-acting insulin compared with insulin glargine. Diabetes Care 2011; 34: 661-665.
- Dzygalo K, Golicky D, Kowalska A, Szypowska A. The beneficial effect of insulin degludec on nocturnal hypoglycaemia and insulin dose in type 1 diabetic patients: a systematic review and meta-analysis of randomised trials. Acta Diabetol 2015; 52: 231-238.
- Lane W, Bailey T, Gerety G, Gumprecht J, Phillis-Tsimikas A, Thim Hansen C, et al. Effect of degludec vs insulin glargine U100 on hypoglycemia in patients with type 1 diabetes. The SWITCH 1 randomized clinical trial. JAMA 2017; 318: 33-44.
- Vora J, Christensen T, Rana A, Bain SC. Insulin degludec versus Insulin Glargine in type 1 and type 2 Diabetes Mellitus: A Meta-Analysis of Endpoints in Phase 3a Trials. Diabetes Ther 2014; 5: 435-446.
- Heller S, Buse J, Fisher M, Garg S, Marre M., Merker, et al. Insulin Degludec, an ultra-long-acting basal insulin, versus insulin glargine in basal-bolus treatment with meal time insulin aspart in type 1 diabetes (BEGIN Basal Bolus Type1): A phase 3, randomised, open-label, treat-to-target, non inferiority trial. Lancet 2012; 379: 1489-1497.
- Nakae R, Kusunoki Y, Katsuno T, Tokuda M, Akagami T, Murai K, et al. Medium-Term Effects of Insulin Degludec on Patients with Type 1 Diabetes Mellitus. Drugs 2014; 14: 133-138.
- Ratner RE, Gough SC, Mathien C, Del Prato S, Bode B, Mersebach H, et al. Hypoglycaemia risk with insulin degludec compared with insulin glargine in type 2 and type 1 diabetes: a pre-planned meta-analysis of phase 3 trials. Diabetes Obes Metab 2013; 15: 175-184.
- Gold AE, MacLeod KM, Frier BM. Frecuency of severe hypoglycemia in patients with type 1 diabetes with impaired awareness of hypoglycemia. Diabetes Care 1994; 17: 697-703.
- Koehler G, Heller S, Korsatko S, Roepstorff C, Rasmussen S, Haahr H, et al. Insulin degludec is not associated with a delayed or diminished response hypoglycemia compared with insulin glargine in type 1 diabetes: a double-blind randomized crossover study. Diabetologia 2014; 47: 40-49.
- Home PD, Meneghini L, Wendish U, Ratner RE, Johansen T, Christensen TE, et al. Improved health status with insulin degludec compared with insulin glargine in people with type 1 diabetes. Diabetes Med 2012; 29: 716-720.
- Woodward A, Weston P, Casson IF, Gil GV. Nocturnal hypoglycemia in type 1 diabetes-frecuency and predictive factors. QJM 2009; 102: 603-607.
- Lane W, Bailey TS, Gerety G, Gumprecht J, Philis-Tsimikas A, Hansen CT. Effect of Insulin Degludec vs Insulin Glargine U100 on Hypoglycemia in Patients With Type 1 Diabetes. The SWITCH 1 Randomized Clinical Trial. JAMA 2017; 318: 33-44.
- Lane W, Bailey TS, Gerety G, Gumprecht J, Philis-Tsimikas A, Hansen CT. Effect of Insulin Degludec vs Insulin Glargine U100 on Hypoglycemia in Patients With Type 1 Diabetes. The SWITCH 1 Randomized Clinical Trial. JAMA 2017; 318: 33-44.
- . Karamat MA, Dar S, Bellary S, Tahrani AA. Clinical and Cost Implications of Insulin Degludec in Patients with Type 1 Diabetes and Problematic Hypoglycemia: A Quality Improvement Proyect. Diabetes Ther 2018; 9: 839-849.
- Pollock R.F, Tikkanen CK. A short-term cost-utility analysis of insulin degludec versus insulin glargine U100 in patients with type 1 or type 2 diabetes in Denmark. J of Med Econ 2017; 20: 213-220.
- Kiss I, Arold G, Roepstorff C, Gammelgaard S, Klim S, Haahr H. Insulin Degludec: Pharmacokinetics in Patients with Renal Impaiment. Clin Pharmacokinetic 2014; 53: 175-183.