Sangrado y terapia hormonal en la menopausia (THM)
Paulina Villaseca D1.
Bleeding during menopause hormone therapy (MHT)
1Departamento de Endocrinología, Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile.
Correspondencia: Paulina Villaseca Edificio Académico ATENTO, Departamento de Endocrinología, 4° Piso, Diagonal Paraguay 386, Santiago Centro, Chile. Correo electrónico: pvillase@med.puc.cl
Recibido: 10-08-2018
Aceptado: 10-11-2018
Resumen: La definición de sangrado ginecológico anormal durante terapia hormonal de la menopausia es aquel sangrado no programado durante el uso de la terapia. Este artículo es un pauteo que describe: 1) cuándo diagnosticar unsangrado anormal, ya que difiere según el tipo de esquema hormonal utilizado; 2) eldiagnóstico diferencial del origen del sangrado anormal; 3) los métodos de evaluación para diagnosticar el origen del sangrado. Se destacan los aspectos principales para el diagnóstico diferencial entre patología orgánica versus disrupción endometrial debida al tratamiento hormonal. Además, se describen los ajustes posibles para resolver el sangrado cuando éste se debe a disrupción del endometrio.
Palabras clave: Cáncer de endometrio; Estrógenos; Hiperplasia endometrial; Menopausia; Pólipo endometrial; Terapia hormonal de la menopausia; Tibolona, Sangrado ginecológico.
Abstract: Abnormal bleeding related to menopausal hormone therapy is defined as unscheduled bleeding during the use of the therapy. This article outlines when to diagnose an abnormal bleeding -as this differs according to the type of hormonal scheme used-, the differential diagnosis of the origin of abnormal bleeding, and the methods of evaluation to assess the origin of the bleeding. The main aspects are highlighted on the differentiation of organic pathology versus disruption of the endometrium due to treatment. Also, treatment adjustments to resolve bleeding when it is due to disruption of the endometrium are outlined.
Key words: Endometrial cancer; Endometrial hyperplasia; Endometrial polyp; Estrogens; Gynecological bleeding; Menopause; Menopause hormone therapy;, Tibolone.
Un sangrado anormal relacionado con la terapia hormonal de la menopausia se define como un sangrado no programado durante el uso de ésta; esto difiere según el tipo de esquema hormonal utilizado:
- Terapia E+P en esquema secuencial cíclico (THMsec):
◊ sangrado extemporáneo al esperado tras el término del progestágeno ◊ sangrado abundante y/o prolongado - Terapia estrógeno –progestativa (E+P) en esquema combinado continuo (THMcc):
◊ sangrado que se inicia o que persiste después de 6 meses de iniciado el esquema
◊ sangrado al inicio del esquema, estando la paciente ya con amenorrea establecida. - Terapia con estrógenos sistémicos solos, sin oposición
progestativa (TE): algunas pacientes, teniendo útero
presente, rechazan la adición de un progestágeno y lo
suspenden.
◊ cualquier sangrado es anormal.
Todo sangrado anormal debe investigarse.
Origen del sangrado anormal: Puede deberse a disrupción del endometrio, a patología benigna, o a morbilidad oncológica ginecológica. La mayoría de las veces el origen es benigno.
El endometrio es el foco principal de evaluación, si bien el sangrado puede también tener su origen en otros tejidos ginecológicos: útero (adenomiosis, miomas), cuello uterino, vagina, y vulva; también en tejidos extraginecológicos: sistema urinario y gastrointestinal.
Patología endometrial
A. Hiperplasia endometrial (HE) y cáncer de endometrio.
La HE es precursora de cáncer de endometrio tipo 1, que es
el que se desarrolla debido a estímulo estrogénico proliferativo,
con histología de tipo endometrioide.
La asociación de morbilidad endometrial con terapia hormonal en la menopausia es variable según el tipo de esquema hormonal en uso:
TE: existiendo útero, la terapia con estrógenos sistémicos
solos, sin oposición progestativa se asocia a:
◊ aumento significativo del riesgo de cáncer: 5x más
que en no usuarias
◊ aumento significativo de HE a los 2 y 3 años, con
evidencia de asociación con la dosis y con la duración
de tratamiento1.
Por ende, siempre debe investigarse el endometrio en caso de sangrado en usuarias de E solos.
- THM E+P: la adición de un progestágeno en mujeres con útero presente, disminuye significativamente el riesgo de HE, con ambos esquemas: combinado continuo y secuencial, al compararlos contra placebo1. Asimismo, no se ha evidenciado diferencias en las tasas de cáncer de endometrio, comparando los esquemas secuenciales con los combinados continuos1.
- E combinado con bazedoxifeno (estrógenos conjugados
de equino (ECE) 0,45 mg + BZA 20 mg/d): esta dosis
de BZD, actuando como antiestrógeno, inhibe la
proliferación endometrial inducida por el estrógeno.
En un año de seguimiento no hubo aumento de HE ni
de cáncer de endometrio, comparado con placebo2;
se esperan estudios a más largo plazo.
• Tibolona (2,5 mg/d): una revisión sistemática Cochrane
describe3:
◊ riesgo de sangrado inesperado: comparado con TH: OR 0,32 (IC 95% 0,24 - 0,41); y comparado con placebo: OR 2,79 (IC 95% 2,1 - 3,7).
◊ riesgo de cáncer de endometrio comparado con TH: OR 1,47, (IC 95% 0,23 to 9,33; y comparado con placebo: OR 2,04 (IC 95% 0,79 - 5,24). Es necesario recordar que la tibolona aumenta en 3 x el riesgo de desarrollar pólipos endometriales4.
B. Pólipos endometriales. Se pueden expresar por sangrado, por tanto, son parte del diagnóstico diferencial de un sangrado anormal durante el tratamiento de la menopausia. No hay claridad sobre su origen y, si bien la gran mayoría son benignos, algunos pueden ser malignos.
Pueden encontrarse como hallazgo ecográfico en aproximadamente un 13% de mujeres post-menopáusicas. No es clara su asociación con la TH de la menopausia, pero sí con el uso de tamoxifeno y de tibolona.
Patología cervical y del canal ginecológico
En caso de sangrado anormal durante TH, siempre se debe evaluar el cérvix uterino con citología de Papanicolau. Habiéndose descartado el origen endometrial del sangrado, se pude proseguir con colposcopía o curetaje endocervical si se considera necesario, según el caso. Asimismo, debe realizarse inspección de vagina y vulva en atención a lesiones.
Métodos de evaluación del endometrio
1. Ultrasonido transvaginal (USTV) convencional (2-D): Este es el primer examen a realizar, permitiendo el diagnóstico tanto de lesiones endometriales como también miometriales (miomas, adenomiosis).
La THMcc causa un endometrio hipotrófico, delgado en la ultrasonografía (Figura 1A).
La THMsec determina un endometrio que difiere en la fase de E solos que en la fase estrógeno-progestativa (similar a lo que ocurre en los ciclos menstruales espontáneos) (Figura 1). Por ello, cuando el esquema de TH es secuencial, debe realizarse el ultrasonido en la fase de estrógenos solos, en que el endometrio debe presentarse como lineal (Figura 1A) o trilaminar (endometrio tipo 1) (Figura 1B). Si en esta fase de estrógenos solos, el endometrio se presenta heterogéneo, con focos de engrosamiento, u homogéneo de tipo 3 (como se observa en la fase progestativa de un ciclo espontáneo o farmacológico) (Figura 1C), debe entonces estudiarse el endometrio.
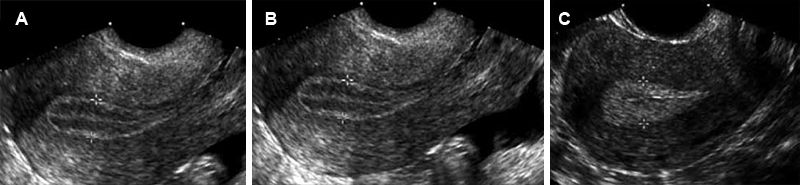 Figura 1. Ultrasonido en las diferentes fases del ciclo menstrual. A: endometrio lineal o hipotrófico. B: endometrio trilaminar – fase folicular del ciclo. C: endometrio homogéneo – fase lútea del ciclo.
Figura 1. Ultrasonido en las diferentes fases del ciclo menstrual. A: endometrio lineal o hipotrófico. B: endometrio trilaminar – fase folicular del ciclo. C: endometrio homogéneo – fase lútea del ciclo.
También es importante la evaluación del grosor del endometrio.
Grosor endometrial por ultrasonido convencional 2-D: El aumento del grosor endometrial se asocia a morbilidad: pólipos endometriales, hiperplasia endometrial, cáncer de endometrio.
El valor umbral de sospecha de hiperplasia/cáncer sería similar al de mujeres sin terapias hormonales.
Existen varios estudios investigando el límite del grosor indicativo de morbilidad, ante un primer sangrado anormal. En dos publicaciones de meta-análisis en mujeres postmenopáusicas con sangrado anormal, se concluyó que un grosor ≤ 5 mm se asocia a una baja posibilidad de cáncer de endometrio (2,3 y 4%), independiente de ser usuaria de TH o no.
Si el sangrado es persistente, se debe proceder a la evaluación del endometrio, independiente de su grosor.
Atención al cáncer de endometrio tipo 2, que puede expresarse por sangrado y grosor endometrial < 4 mm. Este cáncer no es relacionado a estrógenos y la histología es de células claras o serosas; es menos prevalente y tiene mal pronóstico.
La ocurrencia de irregularidades en la imagen morfológica endometrial (USTV) debe ser evaluada dirigidamente, pudiendo realizarse las siguientes técnicas:
2. Ultrasonido transvaginal 3-D y Doppler-color: Tiene la utilidad de detectar el vaso central que nutre un pólipo, apoyando el diagnóstico diferencial en estos casos. No es invasivo.
3. Histerosonografía (HSG): Se indica para precisión diagnóstica ante una lesión focal, pero es un método invasivo (instilación de suero salino en la cavidad endometrial), y puede ser doloroso. El fluido permite un mejor contraste, delineando la lesión focal, logrando mayor precisión para el diagnóstico de miomas submucosos y pólipos endometriales.
La elección es el método previo: USTV 3-D que no es invasivo, y proseguir a realizar la HSG ante la persistencia de la duda de la imagen.
4. Histeroscopía: La visualización directa de la cavidad uterina tiene la ventaja del diagnóstico ante dudas de interpretación de imágenes visualizadas con ultrasonido, por ejemplo: distinción entre pólipo endometrial y mioma submucoso. Esta puede realizarse con histeroscopios de pequeño calibre, sin necesidad de anestesia, pudiendo incluso tomarse una biopsia dirigida.
5. Por último, ante la decisión de la necesidad de evaluar histológicamente el endometrio, se procede a la Biopsia de endometrio: ésta se puede realizar por medio de:
a) cánula de aspiración: ésta es satisfactoria cuando se
percibe el paso de la cánula desde el canal cervical a
la cavidad endometrial y el contenido aspirado permite
una muestra adecuada para análisis histológico.
b) curetaje
c) bajo visión histeroscópica
Las biopsias ciegas por cánula o por curetaje son un método adecuado de pesquisa de cáncer de endometrio y de hiperplasia endometrial, pero no son útiles para el diagnóstico de patología focal ie. pólipos endometriales.
Cuando la muestra no es suficiente para diagnóstico y, el endometrio es >5 mm o el sangrado es persistente, debe procederse a la búsqueda dirigida de una lesión:
6. Resonancia magnética: su utilidad es exclusivamente ante morbilidad específica, en casos en que se requiere definir la extensión de un cáncer de endometrio.
¿Qué hacer ante un sangrado por disrupción del endometrio?
Habiendo ocurrido un sangrado no programado durante el uso de TH en la menopausia, y habiendo descartado un origen específico de éste, se puede asumir que se trata de un sangrado por disrupción del endometrio. El objetivo para su resolución es lograr un balance entre el estrógeno y el progestágeno utilizados:
En caso de THMcc, permitiendo una mayor estabilidad endometrial, sea aumentando la dosis diaria del estrógeno y/o disminuyendo la dosis diaria del progestágeno; también se puede hacer el cambio a un esquema secuencial para lograr un mejor control de sangrado.
En caso de THMsec, ajustando el progestágeno, sea prolongando sus días de acción a 12-14 días o cambiando a una progestina más potente en su acción progestagénica o maduradora del endometrio, como es el acetato de nomegestrol.
Referencias
- Furness S, Roberts H, Marjoribanks J, Lethaby A. Hormone therapy in postmenopausal women and risk of endometrial hyperplasia. Cochrane Database Syst Rev. 2012 Aug 15; VOLUMEN(8): CD000402. doi: 10.1002/14651858.CD000402.pub4.
- Pinkerton JV, Harvey JA, Lindsay R, Pan K, Chines AA, Mirkin S, Archer DF; SMART-5 Investigators. Effects of bazedoxifene/conjugated estrogens on the endometrium and bone: a randomized trial. J Clin Endocrinol Metab 2014; 99: E189-98.
- Formoso G, Perrone E, Maltoni S, Balduzzi S, Wilkinson J, Basevi B, Marata AM, Magrini N, D’Amico R, Bassi C, Maestri E. Short-term and long-term effects of tibolone in postmenopausal women. Cochrane Database Syst Rev 2016 Oct 12; 10: CD008536.
- Pérez-Medina T, Bajo-Arenas J, Haya J, Sanfrutos L, Iniesta S, Bueno B, Castelo-Branco C. Tibolone and risk of endometrial polyps: a prospective, comparative study with hormone therapy. Menopause 2003; 10: 534-537.
- Munro MG, FACOG; The Southern California Permanente Medical Group’s Abnormal Uterine Bleeding Working Group. Investigation of Women with Postmenopausal Uterine Bleeding: Clinical Practice Recommendations. Perm J 2014 Winter; 18(1): 55-70. http://dx.doi.org/10.7812/TPP/13-072
- Dueholm M, Hjorth IM. Structured imaging technique in the gynecologic office for the diagnosis of abnormal uterine bleeding. Best Pract Res Clin Obstet Gynaecol 2017; 40: 23-43.