Caracterización de línea celular de paratiroides humana (RCPTH) y evaluación de tumorigenicidad en ratones NOD/SCID
Patricio Cabané T. MD/PhD1, Patricio Gac E. MD1, Marcos Ramírez P.2, Ricardo Rossi F. MD1, Sofía Oviedo C. MD3, Carmen Romero O. BQ3, Pablo Caviedes F. MD/PhD5, Flavio Salazar-Onfray PhD6, Lorena Salazar A. PhD, Mercedes López N. MD/PhD6, Leonor Moyano S. MD7 y Raúl Caviedes O. MD5
Characterization of human parathyroid cell line (RCPTH) and tumorigenicity evaluation in NOD/SCID
1Cirugía Endocrina, Cabeza y Cuello y
Oncológica General, Hospital Clínico
Universidad de Chile.
2Doctorado en Ciencias Biomédicas.
3Sección Endocrinología, Departamento
Medicina, Hospital Clínico Universidad de Chile.
4Laboratorio Endocrinología y Biología de la
Reproducción, Hospital Clínico Universidad de
Chile.
5Laboratorio de Terapia Celular, ICBM, Facultad
de Medicina Universidad de Chile.
6Laboratorio de Inmunología Antitumoral,
ICBM, Facultad de Medicina Universidad de
Chile.
7Departamento de Anatomía Patológica,
Hospital Clínico Universidad de Chile.
Correspondencia:
Patricio Cabané Toledo, MD/PhD
E-mail: patriciocabane@sqin.cl
www.sqin.cl / www.paratiroides.cl
Recibido: 30 de enero de 2013
Aceptado: 10 de abril de 2013
Background: Cell therapy could be an alternative for the treatment of hypoparathyroidism. Therefore efforts have been made to establish a cell line of parathyroid cells. Aim: To establish a continuous functional and non-tumorigenic human parathyroid cell line. Material and Methods: Nineteen tissue samples from 15 patients subjected to parathyroidectomy due to primary or secondary hyperparathyroidism were obtained. Functional, morphological and tumorigenic properties of the obtained cells were analyzed. Results: After two months of culture in conditions of immortalization, cells had an exponential growth without experiencing senescence. Therefore, more than 200 sub cultures have been performed. The cell line was denominated RCPTH. Morphological characterization showed monolayer growth with contact inhibition and a duplication time of 30 hours. On light microscopy, pleomorphism and low number of mitoses were observed. Cells accumulated glycogen, expressed calcium sensing receptor and had positive PTH cytoplasmic clusters. The line secreted PTH initially but subsequently, PTH production became undetectable. The cell line did not have tumor or metastatic growth. Conclusions: A parathyroid cell line has been established. The lack of PTH production is a problem that will require the search for mechanisms to activate it.
Key words: Parathyroid cell line, tumorigenic, cellular study.
El hipoparatiroidismo permanente ocurre en un 0,2 a 4% de las cirugías de tiroides1.
El tratamiento de esta secuela postoperatoria puede ser médico o quirúrgico. El tratamiento médico considera la administración de calcio y vitamina D a permanencia y en algunos casos incluso el uso de diuréticos. El tratamiento quirúrgico a su vez puede ser intraoperatorio o post-operatorio. El primero consiste en realizar un autotrasplante de glándulas resecadas o dañadas (con 99% efectividad), mientras que en el tratamiento quirúrgico post-operatorio se intenta un autotrasplante de tejido criopreservado del mismo paciente que tiene el inconveniente de que su efectividad disminuye a 50% y se debe contar con un Banco de Criopreservación de Paratiroides. Sin embargo, no siempre es posible contar con el tejido paratiroídeo del paciente, por lo que otra alternativa quirúrgica es el alotrasplante utilizando tejido paratiroídeo de pacientes intervenidos por hiperparatiroidismo secundario2,3.
Los aloinjertos, ya sea de células o tejidos, se han intentado sin inmunosupresión para evitar efectos adversos graves. Se ha logrado mantener una función paratiroídea normal sólo por 18 meses, hasta que los injertos son rechazados4,5. En nuestra experiencia logramos mantener niveles de PTH detectables pero subnormales por 20 meses en una paciente con hipoparatiroidismo severo al alotrasplantar tejidoparatiroídeo microencapsulado, durante el período de funcionamiento del injerto se logro suspender el aporte de calcio endovenoso contínuo y mejorar la calida de vida de la paciente6.
El establecimiento de una línea celular de paratiroides se ha intentado por muchos años con el inconveniente de que la funcionalidad se altera (secreción de PTH y respuesta a niveles de calcio extracelular) y la sobrevida no es muy prolongada (senescencia en 20 sem)7,8,9.
El objetivo de este trabajo fue establecer una línea celular continua de paratiroides humana funcional y no tumorigénica y así lograr ampliar el espectro terapéutico de pacientes con hipoparatiroidismo, con la posibilidad de realizar aloinjertos con una línea celular de paratiroides humana. Con el uso de un método especial de inmortalización, descrito por Caviedes R y cols 199210, se estableció la línea RCPTH la que fue caracterizada morfocinéticamente y funcionalmente, en condiciones de cultivo aislado y de cocultivo con células nodriza (Granulosa Humana). Además se evaluó sus características de proliferación y tumorigenicidad in vitro y tumorigenicidad in vivo mediante injerto en ratones inmunodeficientes (NOD/SCID).
Metodología
Durante el período inicial del estudio, se obtuvo 19
muestras de tejido de 15 pacientes paratiroidectomizados por
hiperparatiroidismo primario o secundario. El estudio fue
aprobado por el comité de ética de la Facultad de Medicina
de la Universidad de Chile, y se desarrolló desde el año 2003.
Se utilizó un consentimiento informado debidamente aprobado
por este comité.
Se excluyó pacientes con antecedentes de infección por virus hepatitis C o B, CMV, VIH, y pacientes con sospecha de cáncer paratiroídeo. Se confirmó la naturaleza benigna de las muestras por biopsia.
Las muestras fueron trasportadas al laboratorio en medio DMEM/F12 (Sigma ®) a 4°C. En el laboratorio, en condiciones de esterilidad bajo campana de flujo laminar, se procedió a disgregar mecánicamente el tejido separando el estroma del parenquima. El parénquima identificado es cortado en piezas de 1 x 1 mm y disgregado enzimáticamente con colagenasa II (Worthington ®) al 0,2% incubando 30 min a 37°C. Posteriormente se disgrega por pipeteo en pipetas de vidrio, se centrifuga para lavar el medio de digestión y se siembra en placas de plástico para cultivo primario con medio DMEM/ F12 suplementado con Suero Bovino Adulto 10%, Suero Fetal Bovino 5% y Gentamicina (4 μgr/ml). Para el proceso de inmortalización se utilizó el método descrito anteriormente11,12. En resumen, se agrega al medio de cultivo primario un medio condicionado por la línea tumoral de tiroides de rata (UCHT1) al 10%. Con esto se logra la transformación en un plazo de 1 a 8 meses.
El medio de cultivo se cambió cada 3 días o según necesidad, por viraje del marcador de pH (rojo fenol). Para los subcultivos se utilizó método enzimático con tripsina 0,2%. Se controló los cultivos por microscopía invertida de contraste de fases.
Una vez establecido el cultivo continuo (paciente con Dg de HPT 1rio-Adenoma de paratiroides) se trabajó en el Laboratorio de Cultivo Celular y en el Laboratorio de Inmunología Tumoral de la Facultad de Medicina Universidad de Chile.
La línea celular obtenida se denominó RCPTH.
Evaluación de la curva de crecimiento de la línea celular continua de paratiroides humana (RCPTH)
Al obtener el crecimiento continuo de la línea se sembró en placas de 6 cm de diámetro 70.000 céls/placa, en duplicado. Se contó el número de células en cámara de neubauer cada 24 h. Se realizó experimento en triplicado.
Método de evaluación de la duplicación celular
Tiempo que demora un cultivo en doblar el número de células. Contando con cámara de neubauer (conteo celular) y según método de Caviedes y cols en placas de 35 mm10.
Conteo celular: Primero se siembran 70.000 células/placa de 6 cm de diámetro en triplicado (15 placas) y se tripsiniza y cuentan las células en cámara de neubauer cada 24 h.
Método Caviedes: Se siembran las células a baja densidad en placa de 35 mm. Se marca puntos de referencia en la placa y en el microscopio. Buscando las mismas coordenadas cada vez, se cuenta el número de células por campo en díassucesivos, según el modelo y fórmula siguiente:
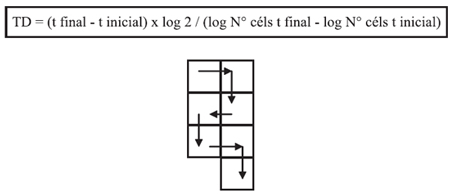
Protocolo de tinción con hematoxilina-eosina
Se sembró las células RCPTH a baja confluencia en placas con cubreojetos. Se incubó con medio de cultivo DMEM/ F12 hasta lograr adherencia. Se retiraron los cubreobjetos y se fijó las células con alcohol 96°. Luego se sumergieron en Hematoxilina de Harris por 2 min. Luego se elimina el exceso de tinción con alcohol ácido al 1%. Se sumerge en Eosina acuosa por 1 min y se elimina el exceso con agua corriente. Se somete los cubreobjetos a batería de alcoholes para deshidratación, se fijan y montan en placas.
Tinción de la reacción del ácido periódico de Schiff (PAS)
Las células de paratiroides humana tienen reacción PASpositiva como pocas células (musculares, renales, hepáticas) ya que tienen un contenido de glicógeno elevado. El ácido periódico oxida los 1,2-glicoles de los tejidos transformándolos en aldehídos que se colorean con el reactivo de Schiff.
Para este experimento se incuban células RCPTH sobre cubreobjetos. Primero se agrega el ácido periódico (0,5% en agua destilada) sobre las células lavadas previamente con PBS, por 5 min. Se lava con agua corriente y luego con agua destilada. Se continúa con la incubación con el reactivo de Schiff (Fucsina básica 1g, HCl N 20 ml, Bisulfato sódico anhídrico 1 g en 200 ml de agua destilada) por 15 min y luego se realizan baños de ácido sulfuroso (Metabisulfito sódico al 10% 6 ml, HCl N 5 ml en 100 ml de agua destilada) por 3 veces (2 min cada vez). Se deshidrata las células en batería de alcoholes y se monta para visualización en microscopio óptico.
Se utilizó hepatocitos de ratas Fisher 344 (línea Gerschenson) como control positivo12,13.
Caracterización por inmunofluorescencia (PTH-CaSR)
Se sembró sobre cubreobjetos de vidrio en placas de 6 cm de diámetro a baja confluencia. Una vez adheridas las células se lavó las placas con PBS. Se fijó con metanol frio (-20°C) por 30 min. Se lava con PBS (3 veces, 5 min cada vez) luego se bloquea con Suero Normal de Caballo 10% por 20 min. Se lava 3 veces con PBS, y se incuba con anticuerpo primario a 4°C toda la noche. Se utilizó anticuerpo anti PTH humana (N-18) de cabra 1:100 (Santacruz Inc) y anti PTH humana de conejo 1:200 (Abcam - ab53040) y Anti CaSR (receptor de calcio sensible) Humano de ratón 1:100 (Chemicon). Luego se lava 3 veces con PBS y se incuba con anticuerpo secundario Anticabra biotinilado (20 μg/ml - Vectorlabs) y Antiratón conjugado con FITC (20 μg/ml - Vectorlabs), por 1,5 h. Se lava con PBS, se montan los cubreobjetos en portaobjetos de vidrio con medio de montaje para fluorescencia (Dako). Se observa fluorescencia en microscopio Karl Zeiss, digitalizando imágenes con cámara Cool Snap sf. Como control positivo se utilizó tejido paratiroídeo criopreservado y cultivado de otros pacientes.
Evaluación de la función endocrina (producción y secreción de PTHi) y curva dosis/respuesta a calcio extracelular
La producción de paratohormona en el medio de cultivo se midió por radioinmunoensayo con el kit Immulite PTHi (DPC). Se sembró en placas de 6 cm de diámetro 70.000 céls/ placa, en duplicado. Una vez logrado el 80% de confluencia se cambió el medio de cultivo por un medio Joklik (sin calcio) suplementado con CaCl2 en concentraciones de 0,5 - 1 - 1,5 - 2 - 3 mM Calcio. Se incubó las placas en duplicado por cada condición por 2 h a 37°C. Luego se obtuvo muestras del medio y se congeló a –20°C para su posterior análisis. Las células fueron lisadas con buffer RIPA para medición de proteínas por el método de Bradford, para la normalización de los resultados.
Mejoramiento de condiciones de cultivo mediante cocultivo con células de granulosa humana
Al avanzar en el tiempo y número de subcultivos la línea celular RCPTH bajó el nivel de producción y secreción de PTH por lo que se intentó mejorar las condiciones de cultivo para optimizar la producción y secreción de PTH.
En otros modelos endocrinos de trasplante celular, se ha intentado mejorar la sobrevivencia y función endocrina de las células en cultivo mediante técnicas de cultivo en suspensión y cocultivos14. Por ejemplo, en estudios utilizando Islotes de Langerhans para terapia de trasplante celular en diabetes mellitus se está pregonando el cocultivo de los Islotes con células nodrizas que aporten factores paracrinos de regulación. Algunos autores han logrado mayor sobrevida de los Islotes y mejor respuesta de secreción de insulina al cocultivar con hepatocitos15 y con células de Sertoli14,16,17. También se ha observado que esta condición de cocultivo protege a los islotes de la destrucción alo y autoinmune18. Incluso, hay experiencias preliminares de xenotrasplantes de estos conglomerados celulares microencapsulados en pacientes con Diabetes Mellitus tipo 1 (12 casos), disminuyendo los requerimientos de insulina en un 40%19.
Dentro de las líneas celulares humanas conocidas como nodrizas están las ya mencionadas células de Sertoli (utilizada en cocultivos con islotes de Langerhans) y las células de granulosa humana. De estas últimas existe una línea celular inmortalizada en nuestro laboratorio (RCGH). (Caviedes y cols. Pat. WIPO Nº WO 03/065999 A2).
Se estableció condiciones de cocultivo de la línea RCPTH y la línea RCGH (granulosa humana), además de condiciones de cultivo con el medio condicionado de esta última. Se determinó proliferación y tiempo de duplicación. No hubo detección de PTH.
Evaluación de proliferación
Se evaluó la proliferación de la línea celular RCPTH en condiciones de cocultivo con una línea celular nodriza y a distintos porcentajes de confluencia de placa. Se estableció el valor de porcentaje de incorporación de BrDU en condición basal y en condición de cultivo mejorado (cocultivo). Además se utilizó inmunocitoquímica anti Ki67 como marcador de proliferación utilizado ampliamente en clínica.
Incorporación de BrDU (bromodeoxiuridina)
Se utiliza células cultivadas sobre cubreobjetos a baja confluencia en triplicado en las distintas condiciones con PBS, dos veces. Se fija las células con Metanol a -20°C por 10 min (mantener a 2-8°C). Una vez seco (al aire) se pueden mantener a -20°C en caja sellada o rehidratar para continuar el procedimiento. Para rehidratar, sumergir en PBS por 3 min. Luego denaturar el DNA incubando placas en HCL 2N a 37°C por 60 min y posteriormente se neutraliza el ácido clorhídrico sumergiendo placas en Buffer Borato 0,1 M pH 8,5 (lavar 2 veces por 10 min c/u). Se lava con PBS 3 veces c/u. Para la incubación del anticuerpo primario (Anticuerpo BrDU mouse (Sigma N° cat. 2.531) diluído 1:1.000), se coloca en cámara húmeda (placa de petri con toalla secante húmeda) y se incuba con el anticuerpo primario por 60 min a T° ambiente. Se lava con PBS por 3 veces, 10 min c/u. Luego se aplica el anticuerpo secundario a dilución 1:100. Anti Mouse-FITC (VectorLabs) diluido en buffer recomendado por el fabricante (NaHCO3 0,1 M, pH 8,5 en NaCl 0,15 M). Se lava con PBS por 3 veces, 10 c/u y finalmente se monta con medio de montaje Dako en portaobjetos. En microscopio se cuenta el número de células totales y con tinción nuclear positiva. Se expresa el porcentaje de células positivas sobre el total. Porcentaje de proliferación.
ICQ para Ki67
Se utiliza células cultivadas sobre cubreobjetos a baja confluencia en triplicado en las distintas condiciones con PBS, dos veces. Se fija las células con Metanol a -20°C por 10 min. Para medir la presencia de Ki-67, se realizó primariamente la recuperación de los antígenos nucleares, mediante incubación en buffer Tris-EDTA, a pH 9, en microondas por 6 min a potencia máxima y 1 h a baja potencia. Se consideró positiva la presencia de marcación para Ki-67 en citoplasma difuso o Golgi, examinando el área de mayor confluencia, se expresa el resultado en porcentaje de células positivas sobre el total de células en 10 campos al azar.
Evaluación de tumorigenicidad
La tumorigenicidad de una línea celular continua se puede determinar por métodos in vitro e in vivo. El Estándar de la caracterización in vitro es la observación del crecimiento celular en condiciones de suspensión celular (sin anclaje- Crecimiento en Agar Blando). Las células tumorigénicas tendrán duplicación celular y formarán colonias, no así una línea no tumorigénica. El estándar de oro de la evaluación de tumorigenicidad in vivo es el injerto de la línea celular en ratones inmunocomprometidos y las observación de éstos por al menos 10 semanas.
Crecimiento en agar blando
Se utilizó esta prueba para evaluar el crecimiento celular
sin anclaje, para evidenciar características tumorigénicas in
vitro. Se agregó Agar al 0,5% suplementado con DMEM/F12
+ Suero fetal bovino al 10% en placas de 3,5 cm de diámetro,
se incubó a 37°C hasta gelificar. Se preparó una suspensión
celular con 5x105 céls/ml en agar 0,3%. Se sembró las células
sobre el agar 0,5% ya gelificado y se incubó por 21 días. Cada
7 días se agregó 200 μlt de medio DMEM/F12 + SFB 10%
para evitar la deshidratación del agar. A los 21 días se contó
el número de colonias (16-50 células) formadas en 10 campos
al azar, confirmando la vitalidad con tripan blue. Se utilizó
como control positivo la línea tumoral Hep2 (carcinoma epidermoide
laríngeo). El experimento fue duplicado en serie.
Tumorigenicidad in vivo
Se utilizó la Línea Celular RCPTH en cultivos estériles libre de micoplasma. Se certificó esta condición por PCR. Se evaluó lo siguiente:
Tumorigenicidad o capacidad de la línea RCPTH de desarrollar tumores en ratones inmunodeficientes, el objetivo es determinar si la línea en un xenotrasplante (células humanas en un ratón), posee o no la capacidad de generar tumor. Se controla el tiempo que les toma generar el tumor y las características del mismo. La inoculación de la línea RCPTH fue por vía subcutánea en los flancos o bordes de la espalda del ratón.
Capacidad Metastásica de la línea RCPTH inoculada, se llevó a cabo una única inoculación por animal (3) con 1 millón de células tumorales en 150 uL de suero fisiológico estéril por vía i.v. en la vena coccígea o de la cola del animal. Para ello los animales son inmovilizados en un cepo acrílico estéril disponible en las dependencias del Bioterio de alta seguridad. La inoculación se llevó a cabo con una jeringa de tuberculina de 31G.
Animales en estudio: 24 ratones (mus musculus, NOD. Cg-Prkdcscid Il2rgtm1Wjl/SzJ, llamados NOD/SCID). Grupo Tumorigenicidad: cuatro ratones fueron inoculados s.c. con 1x106 células RCPTH en un volumen de 150 uL con una jeringa de 1 mL, 31G x 13 mm. El monitoreo del animal y del crecimiento tumoral se realizó diariamente por observación cuidadosa y luego palpación del área inyectada y medición del volumen empleando la fórmula de la elipse: ¶/6 x a x b2, donde a: diámetro mayor y b: diámetro menor.
Grupo Metástasis: Se inoculó vía i.v. en la cola de 2 ratones para evaluar la capacidad metastásica de la línea RCPTH. Los animales se mantuvieron en observación por 6 semanas, luego de las cuales fueron sacrificados para el procuramiento de todos los órganos sólidos toracoabdominales y consiguiente evaluación histopatológica.
Los animales serían sacrificados cuando existiera aparición de tumor de 1 cm o a las 10 sem en caso de inoculación s.c. y a las 6 semanas post-inoculación i.v. La supervisión del bienestar del animal fue llevada a cabo según las normas del Guidelines on the recognition of pain, distress and discomfort in experimental animals and an hypothesis for assessment21.
Grupo Control: Se utilizó 2 ratones como grupo control positivo para cada condición (ratones inoculados s.c. ratones inoculados i.v.). La línea celular de melanoma humano Mel2 (establecida en el Laboratorio de Inmunología Antitumoral) se utilizó como control positivo debido a su capacidad de generar metástasis a distancia. La cantidad de células inoculadas fue una dosis única de 1 x 106 células. Para el Control Positivo de tumorigenicidad por vía s.c. se utilizó la línea PC3 (Ca Prostático humano-Laboratorio de Inmunología Antitumoral-ICBM). Como control negativo se utilizó 2 ratones para cada condición inoculando PBS 1X.
Todos los procedimientos con los ratones fueron llevados a cabo en una sala especialmente acondicionada en el bioterio Central de la Facultad de Medicina Universidad de Chile y por personal entrenado en el manejo de estos animales (Bioterio de Alta Seguridad).
Luego de sacrificados los animales, se disecó la zona injertadapara obtener muestras suficientes para realizar biopsias con tinción corriente H &E y tinción inmunohistoquímica para PTH humana (anticuerpo anti PTH humana (N-18) de cabra 1:100 - Santa Cruz Inc. Y Ac anti PTH Humana abcam ab53040) para detectar células RCPTH.
Cualquier crecimiento macroscópico sería considerado como potencial tumorigénico de la línea celular RCPTH.
En la biopsia se evaluaría mitosis por campo, infiltración tumoral, infiltración vascular y linfática, como marcadores de agresividad del tumor.
Se planificó mediciones regulares de la calcemia y niveles de PTH séricos durante el tiempo de vida de los ratones luego de recibir el injerto, mediante extracciones de sangre de la vena de la cola.
Se realizó medición de los niveles de PTHi en los medios condicionados de cultivos de la línea RCPTH previo a realizar las mediciones in vivo. Si no había detección no se realizaría el injerto.
Análisis estadístico
Se presentan los resultados como promedio ± SD (desviación estándar) de las distintas situaciones experimentales. Para determinar diferencias se utilizó un test no paramétrico para múltiples comparaciones (análisis de varianza, ANOVA) y luego t de Student para comparaciones entre dos grupos. Se utilizó un valor de p < 0,05 como significativo.
Resultados
Establecimiento línea celular
Cultivos celulares de Adenoma de Paratiroides humano con crecimiento continuo, sin senescencia. Se denominó inicialmente como PTH1 y luego se le denominó definitivamente como RCPTH, como una más de las líneas obtenidas en el laboratorio de cultivo de tejidos por el método de Caviedes y cols10 (Figura 1).
 Figura 1. Se observa el crecimiento en monocapa de las células, sin sobrecrecimiento.
Se evidencian mitosis aisladas. Los cultivos se pueden mantener más de
200 días en una placa sin senescencia, ni desprendimiento. Manifiestan inhibición
por contacto al llegar a confluencia total.
Figura 1. Se observa el crecimiento en monocapa de las células, sin sobrecrecimiento.
Se evidencian mitosis aisladas. Los cultivos se pueden mantener más de
200 días en una placa sin senescencia, ni desprendimiento. Manifiestan inhibición
por contacto al llegar a confluencia total.
Curva de crecimiento y duplicación celular
La línea celular RCPTH tiene una curva de crecimiento exponencial y tiempo de duplicación (tiempo en que dobla el número de células en cada placa) de 30 h (Figura 2).
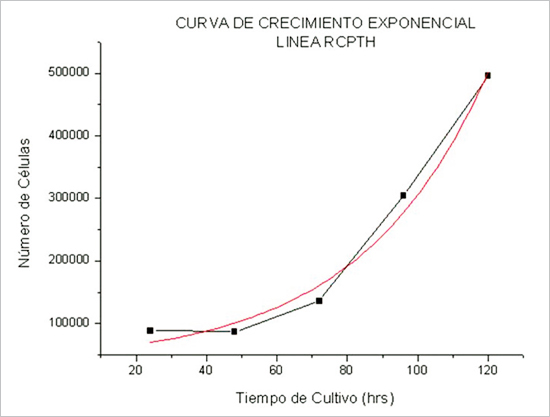 Figura 2. Curva de crecimiento de línea RCPTH (línea continua de paratiroides
humana).
Figura 2. Curva de crecimiento de línea RCPTH (línea continua de paratiroides
humana).
Tiempo de duplicación en cocultivo
Para evaluar con mayor detalle el efecto del medio condicionado
de una célula nodriza (RCGH-línea celular derivada
de granulosa humana) sobre las células RCPTH se consideró
sólo las primeras horas (24-96 h). En este experimento se
logró evidenciar una diferencia significativa del tiempo de
duplicación, siendo mayor en la línea RCPTH sometida a la
exposición a medio condicionado de RCGH. La diferencia es
estadísticamente significativa hasta las 72 h (p < 0,01/n = 3).
El efecto pareciera ir disminuyendo en el tiempo (Figura 3).
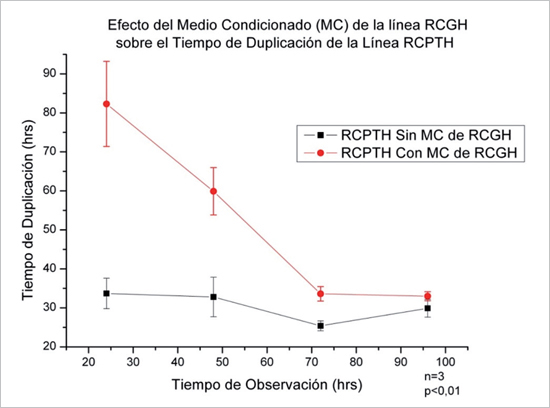 Figura 3. Tiempo de duplicación de la línea RCPTH con y sin exposición al
medio condicionado de la línea RCGH. La curva inferior muestra el comportamiento
habitual de la línea RCPTH (TD promedio de 30 h). (n = 3/p < 0,05).
Figura 3. Tiempo de duplicación de la línea RCPTH con y sin exposición al
medio condicionado de la línea RCGH. La curva inferior muestra el comportamiento
habitual de la línea RCPTH (TD promedio de 30 h). (n = 3/p < 0,05).
Tinción de la reacción del ácido periódico de Schiff (PAS)
En el organismo humano existen sólo cuatro tipos celulares que almacenan Glicógeno (músculo, riñón, hígado, en cultivos celulares en adhesión. Como control positivo se utilizó la línea Gerschenson (hepatocitos de rata Fisher 344). Ambas líneas celulares resultaron positivas para esta tinción. En las placas de la línea celular RCPTH se encontraron células que no resultaron positivas, que actuaron como control interno negativo (Figura 4). Estos distintos tipos celulares puede dar cuenta de la presencia de distintas poblaciones en la línea celular RCPTH (céls. oxifilicas, principales y claras).
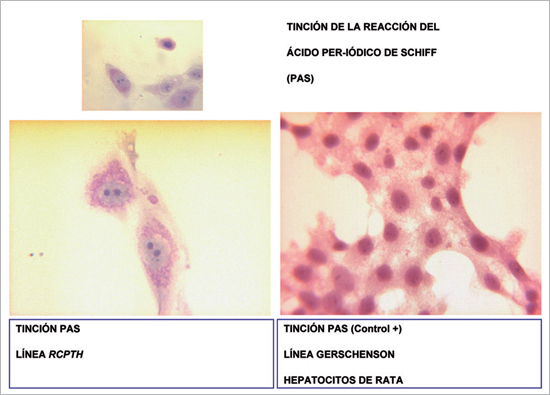
Figura 4. Tinción de la reacción de ácido periódico de Schiff (PAS). Se observa la tinción de glicógeno almacenado en el citoplasma celular. A la derecha se observa la línea de hepatocitos de rata (Gerschenson) como control positivo. 40X.
Inmunocitoquímica (ICQ) anti PTH humana y Receptor de Calcio sensible (CaSR)
Para certificar que las células en crecimiento correspondieran a tejido paratiroídeo funcionante se realizó tinción de inmunohistoquímica para PTH humana y Receptor de Calcio Sensible (CaSR). En la inmunohistoquímica anti PTH se observa el característico patrón granular citoplasmático observado en las líneas primarias (Figura 5). Llamó la atención la presencia de células negativas para esta tinción (control interno negativo), que pueden corresponder a células oxífilas o células claras. La tinción para CaSR presenta un patrón característico de membrana.
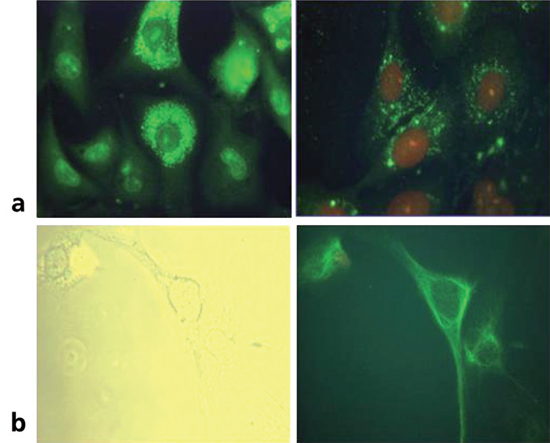 Figura 5. Tinción Inmunohistoquímica. a) PTH: a la izquierda se observa la tinción positiva para PTH de Líne A la derecha se presenta
el control positivo de líneas primarias de paratiroides humana. b) CaSR: Tinción positiva para receptor de calcio sensible en células RCPTH. 40X a celular RCPTH. Llama la atención presencia de células negativas (células oxifilas, claras).
Figura 5. Tinción Inmunohistoquímica. a) PTH: a la izquierda se observa la tinción positiva para PTH de Líne A la derecha se presenta
el control positivo de líneas primarias de paratiroides humana. b) CaSR: Tinción positiva para receptor de calcio sensible en células RCPTH. 40X a celular RCPTH. Llama la atención presencia de células negativas (células oxifilas, claras).
Evaluación funcionalidad
Secreción de PTH
Una vez certificada la naturaleza de las células en cultivo,
vale decir, células productoras de PTH humana y con
expresión del receptor CaSR en la membrana, se procedió a
evaluar la funcionalidad de las mismas. Para ello se midió la
concentración de PTH en el medio (PTH secretada) frente a
distintas concentraciones de calcio extracelular. Es así como a las 2 h de incubación por cada condición se obtuvo los valores
representados en el siguiente gráfico. Normalizados por cantidad
de proteínas por placa (Figura 6).
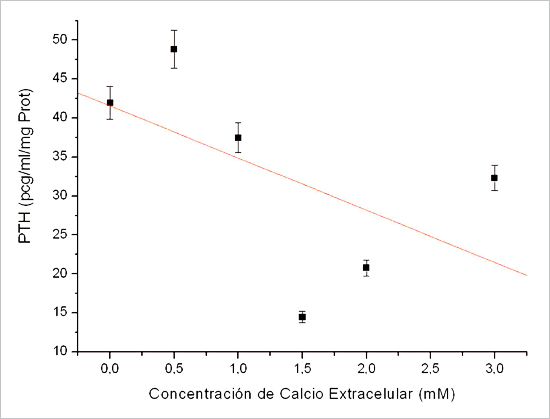 Figura 6. Curva dosis/respuesta de secreción de PTH vs concentración de calcio
en el medio extracelular, Línea RCPTH. Normalizado por mg de proteínas (n = 2).
Figura 6. Curva dosis/respuesta de secreción de PTH vs concentración de calcio
en el medio extracelular, Línea RCPTH. Normalizado por mg de proteínas (n = 2).
Realizando una regresión lineal con el Software Origin 7.0 pro, se obtuvo la curva de tendencia (en rojo), que demuestra que a mayor concentración de calcio extracelular, menor es la secreción de PTH en el medio.
Luego de más de 200 subcultivos la línea celular comenzó a disminuir la secreción de PTH en el medio. Se realizó un experimento aislado de medición de PTHi con kit immulite (DPC)® en medio condicionado (sobrenadante) de cultivos primarios de paratiroides humana (hiperplasia paratiroídea), cultivos de la línea RCPTH y medio de cultivo sólo como blanco. Los resultados son categóricos demostrando que la línea RCPTH perdió la capacidad de secreción in vitro (Tabla 1).
Tabla 1.
Medición de PTHi humana por kit de radioinmunoensayo Roche® en cultivos primarios de paratiroides vs Línea RCPTH. Línea RCPTH con más de 200
subcultivos

Para certificar estas mediciones, nos contactamos con la Dra. Ming Lu, del grupo de investigación liderado por el Dr. Robert Bräntröm del Instituto Karolinskaen Suecia, quienes han realizado importantes estudios en esta área. Ellos aceptaron colaborar con nosotros y les enviamos la línea RCPTH para ser estudiada en su laboratorio. Cuentan con un sistema de perfusión continua de medio, mediante el cual se pueden variar las concentraciones de Ca+2 y recolectar la cantidad de PTH producida por células de paratiroides.
Se utilizó 1x105 células RCPTH, cargadas dentro de una columna conteniendo 3/5 del volumen con gel P-4. La columna fue cuidadosamente cerrada y puesta en una incubadora a 37°C. Para perfundir la columna, se utilizó una bomba peristáltica a una velocidad de 500 uL/3 min. Antes de cada experimento se perfundió medio extracelular con 1,5 mM de Ca+2 y aminoácidos. Luego se perfundió Ca+2 a concentraciones de: 0 mM, 0,5 mM, 1,2 mM, 2,5 mM. Las muestras fueron colectadas cada 3 min y congeladas a -20°C hasta la medición de PTH. Cada experimento fue realizado por triplicado.
La medición de PTH intacta fue realizada mediante un ensayo de electroquimioluminicencia (Roche, Cat. No. 11972219) (Tabla 2).
Tabla 2.
Curva dosis/respuesta de secreción de PTH vs calcio en sistema de perfusión continua (experimento realizado
en Karolinska Institutet, Dra. Ming Lu)
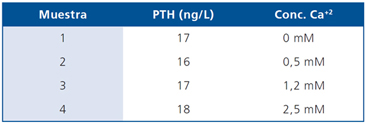
Valores menores a 20 son considerados negativos, por lo que se deduce que no fue posible medir secreción de PTH mediante este sistema.
Una posibilidad es que después de muchos pasajes la línea haya dejado de secretar PTH, que es concordante con nuestros resultados.
Por esta razón se intentó mejorar las condiciones de cultivo
con co-cultivos. Debemos continuar en la búsqueda de las
condiciones de estímulo de producción y secreción de PTH.
Pérdida de producción y secreción de PTH
La línea RCPTH ha tenido más de 200 subcultivos. En los presentes resultados no logramos detectar niveles importantes de PTHi en el medio de cultivo y tampoco evidencia de presencia de PTH intracelular. Se realizó tinción de inmunoflourescencia con Anticuerpo anti PTH humana (Abcam ab53040) con control positivo de cultivo primario de muestra de hiperplasia de paratiroides obtenido de un paciente con insuficiencia renal sometido a paratiroidectomía subtotal (Figura 7).
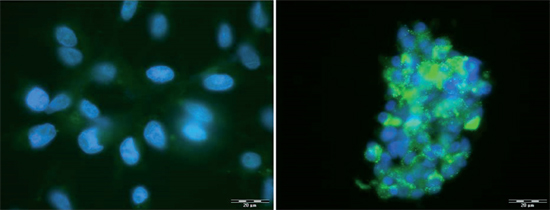 Figura 7. Inmunohistoquímica con anticuerpo Anti PTH humana (Abcamab53040).
40X. Marcación nuclear DAPI. Izquierda: línea RCPTH, no se observa
marcación citoplasmática. Derecha: Cultivo primario de hiperplasia de paratiroides,
Intensa marcación granular citoplasmática.
Figura 7. Inmunohistoquímica con anticuerpo Anti PTH humana (Abcamab53040).
40X. Marcación nuclear DAPI. Izquierda: línea RCPTH, no se observa
marcación citoplasmática. Derecha: Cultivo primario de hiperplasia de paratiroides,
Intensa marcación granular citoplasmática.
Evaluación proliferación
Uno de los objetivos del proyecto es evaluar la tumorigenicidad de la línea RCPTH con el fin de establecer su posible uso en terapia celular. Primero caracterizamos la proliferación in vitro en distintas condiciones (incorporación de BrDU con y sin modificación del medio de cultivo) y con un marcador de proliferación utilizado en clínica (Ki67).
Hasta ahora hemos visto que la línea celular tiene mitosis aisladas en la observación directa de las placas de cultivo. El porcentaje de incorporación de BrDU en condiciones estándar no es muy elevado, concordante con la observación previa. El medio condicionado de la línea RCGH aumenta el tiempo de duplicación en las células de paratiroides humana (Figura 8). Esto se corroboró estudiando el porcentaje de células que incorporan BrDU, traduciendo que este aumento del TD es por disminución de la proliferación (Figura 9).
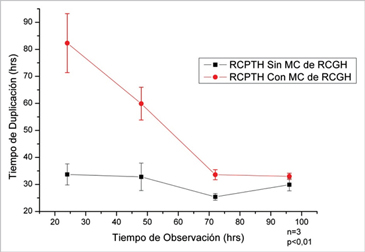 Figura 8. Tiempo de duplicación de la línea RCPTH con y sin exposición al medio
condicionado de la línea RCGH. La curva inferior muestra el comportamiento
habitual de la línea RCPTH (TD promedio de 30 h) (n = 3/p < 0,05).
Figura 8. Tiempo de duplicación de la línea RCPTH con y sin exposición al medio
condicionado de la línea RCGH. La curva inferior muestra el comportamiento
habitual de la línea RCPTH (TD promedio de 30 h) (n = 3/p < 0,05).
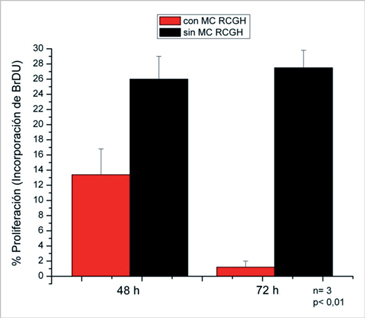
Figura 9. Proliferación de línea RCPTH con y sin exposición al medio condicionado de línea RCGH. La exposición al medio condicionado de RCGH disminuye significativamente la proliferación de la línea RCPTH.
Evaluación tumorigenicidad in vitro e in vivo
Esta característica se evidencia mediante la observación
morfocinética (inhibición por contacto), la proliferación celular
al sembrar en geles de agar blando (independiente de anclaje) y el comportamiento en el injerto en ratas inmunosuprimidas
(nude mice o NOD/SCID).
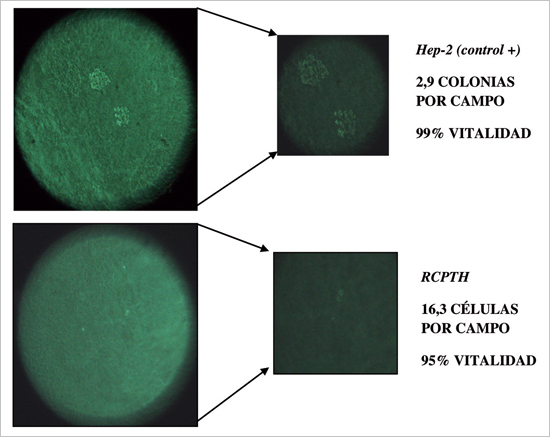
Al permitir el crecimiento de la línea RCPTH en agar blando
por 21 días, no se observó el desarrollo de colonias celulares
(definidos como grupos de 10 a 50 células). Como control
positivo se utilizó una línea celular tumorigénica, Hep-2 (carcinoma
epidermoide laríngeo), donde sí se observó formación
de colonias (aprox. 3 colonias por placa). Este experimento se
realizó en duplicado en forma consecutiva. Se certificó la vitalidad
de las células mediante tinción de azul tripán (Figura 10).
Se evaluó la tumorigenicidad o capacidad de la línea
RCPTH de desarrollar tumores en ratones inmunodeficientes
NOD/SCID. La inoculación de la línea RCPTH fue por vía
subcutánea en los flancos y por vía i.v. en las venas laterales
de la cola del animal.
Inyección subcutánea de la línea RCPTH y línea control (PC3)
En el grupo de tumorigenicidad, cuatro ratones fueron inoculados s.c. con 2x106 células RCPTH en un volumen de 200 uL con una jeringa de 1 mL, 31 G x 13 mm. La inoculación de la línea RCPTH fue por vía subcutánea en los flancos. El monitoreo del animal y del crecimiento tumoral se realizó diariamente por observación cuidadosa y luego palpación en el área inyectada. No se obtuvo crecimiento tumoral luego de 10 sem de haber inyectado las células de paratiroides. Para el grupo control se utilizaron 2 ratones como grupo control positivo en los cuales se inyectó la línea celular de cáncer de próstata PC3. La cantidad de células inoculadas fue una dosis única de 2x106 células. Como control negativo se utilizaron 2 ratones inoculando PBS 1X. Se observó crecimiento de tumores sólidos en el área inyectada con la línea PC3.
Inyección intravenosa de la línea RCPTH (1 x 106) n = 2 y control (Mel2) (1 x 106) n = 2
Grupo Mestástasis: Para determinar la capacidad metastásica de la línea RCPTH, se llevó a cabo una única inoculación por animal con 1 millón de células de la línea RCPTH (2 ratones) y un millón de células de la línea de melanoma Mel2 (2 ratones), en 100 uL de suero fisiológico estéril por vía i.v. en las venas laterales de la cola del animal. Como control negativo, se inyectó 100 uL de suero fisiológico (2 ratones). Se dio un plazo de 6 sem para luego sacrificar los animales y examinar los pulmones. No se detectó metástasis luego de seis sem de la inyección intravenosa de células RPPTH.
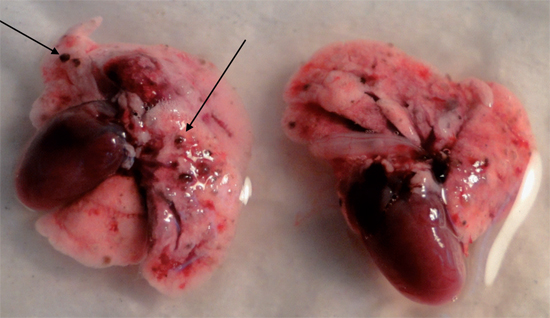
En el grupo control se llevó a cabo una única inoculación por animal con 1 millón de células de la línea de melanoma Mel2, en 100 uL de suero fisiológico estéril por vía i.v. en las venas laterales de la cola del animal. Fue necesario sacrificar los animales luego de 15 días de la inyección de las células de melanoma. Se observaron múltiples nódulos intra y extra pulmonares, de hasta 1 mm de diámetro de color café-negro y bordes irregulares (Figura 11).
Discusión
La obtención de una línea celular continua de paratiroides
humana ha sido un objetivo difícil de conseguir durante
años. Algunos autores han obtenido líneas celulares endoteliales
de tejido paratiroídeo, sin función endocrina7.
En nuestra experiencia, gracias al método de inmortalización utilizado, logramos obtener una línea celular de paratiroides humana con crecimiento exponencial, expresión del receptor de calcio sensible y producción de PTH humana intracelular Esto certifica su naturaleza y el potencial funcional. Además se certificó la secreción de PTH humana al medio extracelular y una tendencia a la disminución si los niveles de calcio extracelular aumentan (función normal).
Sin embargo, como es habitual en las líneas celulares mantenidas en cultivo, la producción y secreción de PTH humana en la línea RCPTH disminuyo hasta ser indetectable. Se intentó establecer condiciones mejoradas de cultivo (cocultivo con células nodriza) sin lograr establecer funcionalidad de la línea en estas condiciones. Podemos elucubrar que al disminuir la proliferación celular estando en contacto con producto secretados por una célula nodriza (factores presentes en el medio condicionado de células de granulosa humana) signifique que mejora su diferenciación y posiblemente su funcionalidad endocrina, como ocurre en otros modelos celulares. Debemos corroborar esta hipótesis en proyectos futuros.
A pesar de la pérdida de la función de la línea celular RCPTH, reportamos la única línea celular humana de paratiroides con mantención de sus características por tanto tiempo de cultivo y con evidencias categóricas de que no es tumorigénica.
La Food and Drugs Adminitration (FDA) de EEUU exige
que cualquier línea celular que se intente utilizar en terapia celular debe tener un test de tumorigenicidad in vivo en ratones
inmunosuprimidos que no tendrán rechazo a las células
injertadas por el compromiso inmunitario de base. Los ratones
NOD/SCID son cepas de difícil cuidado y mantención.
La única cepa de ratones inmunosuprimidos NOD/SCID están
disponibles en el Bioterio de la Facultad de Medicina de
la Universidad de Chile. En Chile era imposible realizar esta
metodología hasta hace un tiempo, sin embargo, debido al
desarrollo de la investigación en Inmunología Antitumoral,
se logró establecer las condiciones necesarias para mantener
cepas de estos animales con seguridad.
La línea RCPTH demuestra en diversos análisis no tener característica de célula tumoral. Crece en monocapa, tiene inhibición por contacto, tiene baja tasa de mitosis, bajo porcentaje de incorporación de análogos de timidina (BrDU) y no presenta formación de colonias en condiciones de suspensión celular (crecimiento en agar blando).
En la prueba de tumorigenicidad in vivo se probó mediante la observación durante 10 sem que no produce tumores subcutáneos en ratones NOD/SCID y tampoco tiene potencial metastático hematógeno.
Debemos establecer en el futuro condiciones de cultivo que estimulen la producción y secreción regulada de PTH humana.
Estas observaciones y pruebas científicas apoyan el establecimiento de una línea celular de paratiroides humana única, sin potencial tumorigénico, que podría utilizarse en el futuro en terapia celular.
Agradecimientos
A la SOCHED, por el aporte de recursos mediante fondo
concursable SOCHED Nº 2010-05 para la realización del
proyecto “Tumorigenicidad in vivo de línea de paratiroides humana”. A la Oficina de Apoyo a la Investigación Clínica
(OAIC): por la asesoría metodológica y acreditación de protocolos.
A Edgardo Caamaño, Laboratorio Endocrinología y
biología de la reproducción, HCUCH por su apoyo constante
en la medición de PTH.
Referencias bibliográficas
- Gac P, Cabané P, Amat J y cols. 2007. Hipocalcemia post Tiroidectomía Total. Rev Med Chile 135: 26-30.
- Kald BA, Mollerup CL. 2002. Risk factors for severe postoperative hypocalcemia alter operations for primary hyperpaarthyroidism. Eur J Surg 168 (10): 552-556.
- Olson J, De Benedetti M, Baumann D, Wells S. 1996. Parathyroid Autotransplantation during thyroidectomy. Ann Surg 223: 472-480.
- Tolloczko T, Wozniewicz B, Sawicki A, Nawrot I, Migaj M, Zabitowska T, Gòrski A. 1994. Cultured parathyroid cell transplantation without immunosupression in the treatment of surgical hypoparathyroidism. Tranplantation Proceedings 26 (4): 1901-1902.
- Tolloczko T, Wozniewicz B, Sawicki A, Gòrski A. 1997. Allotransplantation of Cultured Human Parathyroid Cells: Present Status and Perspectives. Transp Proc 29: 998-1000.
- Cabané P, Gac P, Amat J, Pineda P, Rossi R, Caviedes R, Caviedes P. 2009. Allotransplant of microencapsulated parathyroid tissue in severe postsurgical hypoparathyroidism: a case report. Transplant Proc 41 (9): 3879-3883.
- Brandi ML, Fitzpatrick LA, Coon H, Aurbach G. 1986. Bovine parathyroid cells: cultured maintained for more than 140 population doublings. PNAS 83: 1709-1713.
- Picariello L, Benvenuti S, Recenti R, Formigli L, Falchetti A, Morelli A, et al. 2001. Microencapsulation of human parathyroid cells: An “in vitro” study. J Surg Res 96: 81-89.
- Nawrot I, Wozniewicz B, Tolloczko T, Sawicki A, Gorski A, Chudzinski W, et al. 2007. Allotransplantation of cultured parathyroid progenitor cells without immunosuppression: clinical results. Transplantatio 83 (6): 734-740.
- Caviedes R, Liberona JL, Hidalgo J, Tascon S, Salas K, Jaimovich E. 1992. A human skeletal muscle cell line obtained from an adult donor. Bioch Biophys Acta 1134: 247-255.
- Cabané P, Oviedo S, Romero C, Rossi R, Caviedes R, Caviedes P. 2003. Cultivo primario e inmortalización de células de paratiroides para trasplante celular en hipoparatiroidismo postquirúrgico. Rev Chil Cirugía 55 (6): 617-621.
- Cabané P, Rossi R, Oviedo S, Romero C, Caviedes R, Caviedes P. 2006. Primera Línea Celular Inmortal de Paratiroides Humana. Revista HCUCh 17 (1): 13-19.
- Gerschenson LE, Andersson M, Molson J, Okigaki T. 1970. Tyrosine Transaminase Induction by Dexamethasone in a New Rat Liver Cell Line. Science 170: 859-861.
- Cameron D, Hushen J, Nazian S. 2001. Formation of insulin-secreting, sertoli enriched tissue constructs by microgravity coculture of isolated pig islets and rat sertoli cells. In vitro Cell Develop Biol 37 (8): 490-498.
- Soto ML, Del Río R, Álvarez S, Martin MS, Jara A. 2001. Co-trasplante alogénico de células hepáticas e islotes en ratas diabéticas. Mapfre Medicina 12 (3): 198-203.
- Garkavenko O, Elliott RB, Escobar L, Muzina M. Diatranz Ltd. Growing cells for xenotransplantatio in culture. 20th Annual Scientific Meeting, Canberra, Australia 2002. The transplantation society of Australia.
- Korbutt GS, Elliot JF, Rajotte RV. 1997. Cotransplantation of allogeneic islets with allogeneis testicular cell aggregates allows long-term graft survival without systemic immunosupression. Diabetes 46 (2): 317-322.
- Suárez-Pinzon W, Korbutt GS, Power R, Hooton J, Rajotte R, Rabinovitch A. 2000. Testicular Sertoli cells protect islets (beta)- cells from autoimmune destruccion in NOD Mice by transforming growth factor-(beta)1-dependent mechanism. Diabetes 49: 1810- 1818.
- Valdés R, Elliot R, Garibay N, Garvavenko D, Bracho E, Macias C, et al. Safety and preliminary efficacy of porcine islets and sertoli cells implanted into an autologous collagen generatin device in type 1 diabetic humans. 5th International Congress of the Immunology of Diabetes Society 2001. Concurrent Session: Cell and Islet xenotransplantation. Chicago, IL, USA. 29 sept-03 oct 2001.
- Caviedes P, Caviedes R, Freeman TB, Sanberg PR, Cameron DF. Proliferated Cell Lines and Uses Thereof. International Publication number WO 03/065999 A2. Filed feb. 8th, 2002, publication date: August 14th, 2003. World Intellectual Property Organization, International Bureau. USA: US 2003/0232752 A1 (7 feb 2003). European Patent EP1575524 (09/21/2005).
- Morton DB, Griffiths PH. 1985. Guidelines on the recognition of pain, distress and discomfort in experimental animals and an hypothesis for assessment). The Veterinary record 116: 431-436.