Lectura crítica de estudios de asociación genética en enfermedades complejas
Jorge Sapunar Z.1
Critical reading of genetic association studies in complex diseases
1Centro de Excelencia CIGES. Unidad de Endocrinología, Departamento de Medicina Interna, Facultad de Medicina.
Universidad de La Frontera. Temuco.
Correspondencia:
Jorge Sapunar Zenteno Msc
Antumalal 01024. Temuco.
E-mail: jsapunar@ufro.cl
Recibido: 15 de mayo de 2012
Aceptado: 24 de mayo de 2012
Introducción
Una enfermedad es compleja cuando su patogenia depende de la interacción de múltiples factores genéticos entre sí y con múltiples factores ambientales. En Endocrinología son enfermedades complejas aquellas que constituyen los mayores problemas de Salud Pública como la obesidad común, síndrome metabólico, diabetes mellitus 2, síndrome de ovarios poliquísticos, las dislipidemias y neoplasias endocrinas más frecuentes. Las variantes genéticas más frecuentemente estudiadas en enfermedades complejas son los polimorfismos de un solo nucleótido (SNPs).
El desarrollo de tecnologías de genotipificación costoefectivas ha puesto a disposición del lector miles de artículos de asociación genética en enfermedades complejas. La mayor parte de los estudios comunicados son del tipo gen candidato, establecen asociaciones entre SNPs y fenotipos relacionados con enfermedades complejas.
El riesgo del desenlace clínico atribuible al haplotipo de susceptibilidad suele ser pequeño (OR < 1,2). La frecuencia de los haplotipos de susceptibilidad en las muestras estudiadas es muy variable. La replicación posterior de los resultados, en estudios con poblaciones independientes, fracasa con frecuencia. Todos estos hechos explican las crecientes exigencias metodológicas a los estudios de asociación genética por parte de los Comités Científicos de las principales revistas biomédicas. También obligan al lector, particularmente si es un médico clínico, a manejar herramientas para evaluar la calidad metodológica de los estudios de asociación genética aunque no cuente con formación en ciencias fundamentales.
Objetivo de la guía de lectura
- Conocer los factores que explican la baja reproducibilidad de los estudios de asociación genética.
- Entregar algunas recomendaciones para la lectura crítica de artículos de asociación genética.
Diseñando un estudio de asociación genética
De un punto de vista epidemiológico los autores de un
estudio de asociación genética se formulan la siguiente pregunta
de investigación:
¿Cuál es el efecto de la(s) variante(s) genética(s) X en el riesgo de expresar el (los) fenotipo(s) Y en los sujetos Z considerando variables de control?
Esta pregunta da origen a 2 tipos de objetivos:
- Comparar frecuencias alélicas entre sujetos con y sin el
desenlace:
Ha: ƒ AA (enfermos) > ƒ AA (no enfermos)
- Comparar la frecuencia del desenlace entre sujetos con y
sin el haplotipo de susceptibilidad:
Ha: ƒ E (AA) > ƒ E (Aa, aa)
Donde Ha es hipótesis alternativa y ƒ es la frecuencia.
La Tabla 1 resume los posibles hallazgos de un estudio de asociación genética.
Los estudios de asociación genética se pueden clasificar
de acuerdo a su vinculación con una hipótesis:
- Estudios de asociación de genes candidatos: Evalúan la
hipótesis alternativa de que alteraciones en uno o más
genes de una vía específica se asocian con la enfermedad
de interés o desenlaces relacionados.
- Estudios de asociación genética amplia (GWA): Es un análisis de variación genética conducido sin hipótesis para detectar genes asociados por frecuencia a la enfermedad de interés o desenlaces relacionados
Independientemente que éste corresponda a un estudio de gen candidato o GWA, puede ser diseñado como:
- Estudio de corte transversal: Este tipo de estudio utiliza
los datos extraídos de una muestra representativa de la
población de interés. Comunica el estado de un individuo
de la muestra en términos de la presencia o ausencia de
una variante genética para un determinado desenlace y
la presencia o ausencia del mencionado desenlace en un
tiempo determinado. Para exposiciones que persisten inalteradas
en el tiempo (Género, etnia, genotipo), los estudios
de corte transversal pueden establecer asociaciones
estadísticas válidas. En la Tabla 1 se puede apreciar que
la frecuencia (prevalencia) del desenlace en los expuestos
es A/A+B y la frecuencia del desenlace en los no expuestos
es C/C+D. La Razón de Prevalencia (RP) es el
cuociente entre la frecuencia del desenlace en los expuestos
y la frecuencia del desenlace en los no expuestos. RP
describe la magnitud de la asociación entre exposición y
desenlace siempre y cuando la exposición sea inherente
al individuo (Género, etnia, genotipo).
Los estudios de corte transversal tienen ventajas como no tener limitaciones de tiempo y poder aportar frecuencia (Prevalencia) total y por subgrupos. Sin embargo tienen limitaciones importantes como el requerir de gran tamaño muestral y que la estimación de frecuencia sólo es válida si se cuenta con una muestra representativa de la población.
- Estudios de cohortes: Este tipo de estudio selecciona a
los sujetos a partir de tener o no la variante genética para
luego seguirlos en el tiempo registrando la ocurrencia del
desenlace (Cohorte Prospectiva) o registrando el antecedente
de haberlo tenido (Cohorte Retrospectiva), como
lo muestran las Figuras 1 y 2. En la Tabla 1 se puede
apreciar como un estudios de cohortes permite estimar
la incidencia del desenlace. La magnitud de asociación
(Riesgo), debido a la secuencia temporal se establece
mediante Riesgo Relativo (RR) o Riesgo Absoluto (RA).
RR = A/A +B/C/C + D
RA = (A/A + B)- (C/C+D)
Ej. RR de 2 significa que el riesgo de tener el desenlace en los sujetos con la variante genética es 2 veces mayor que en aquellos que no la tienen. Los estudios de cohortes son óptimos en exposiciones raras (Variantes infrecuentes), permiten examinar más de un desenlace a la vez y entregan la incidencia del desenlace en expuestos y no expuestos. Sin embargo, son ineficiente con desenlaces raros y de latencia larga, casi siempre requieren de gran tamaño muestral y son demandantes de tiempo.
- Estudios de casos y controles: Este tipo de estudio selecciona
a los sujetos a partir del desenlace, es decir los
casos serán aquellos con el fenotipo de interés y los controles
aquellos sin el desenlace. En ambos grupos se investigará
la presencia de la (s) variante (s) genética(s).
En la Figura 3 se puede apreciar la secuencia temporal de un estudio de asociación genética de casos y controles. En la Tabla 1 se puede apreciar como la magnitud de asociación (Riesgo) se establece mediante Razón de Odds (OR).
OR = A x D/B x C
Ej. OR de 2 significa que el riesgo de encontrar la variante genética en los sujetos con el desenlace es 2 veces mayor que en aquellos sin el desenlace. Los estudios de casos y controles requieren de tamaño muestral relativamente pequeño determinado por la frecuencia del haplotipo. Son óptimos para enfermedades poco frecuentes, latencia prolongada y permiten evaluar exposiciones múltiples (GWA). Por estas razones este diseño es el favorito en estudios de asociación genética.
Una vez elegido el diseño del estudio de asociación genética debemos establecer el tamaño de la muestra. Considerando que el diseño de elección es casos y controles, el tamaño muestral dependería de:
- Frecuencia alelélica.
- Nivel de significancia.
- Poder estadístico.
- Magnitud del efecto.
El tamaño disminuye en la medida que aumenta la frecuencia del alelo de susceptibilidad y el tamaño del efecto (OR alélico). En la Tabla 2 se puede apreciar el tamaño muestral requerido de acuerdo a la frecuencia alelélica.
Tabla 1.
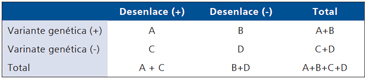
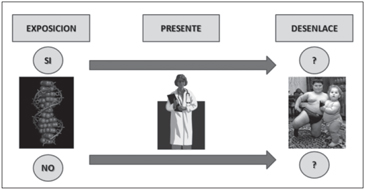 Figura 1. Estudios de cohortes prospectivo secuencia temporal.
Figura 1. Estudios de cohortes prospectivo secuencia temporal.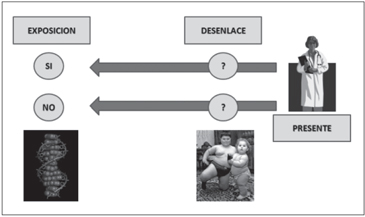 Figura 2. Estudios de cohortes retrospectivo secuencia temporal.
Figura 2. Estudios de cohortes retrospectivo secuencia temporal.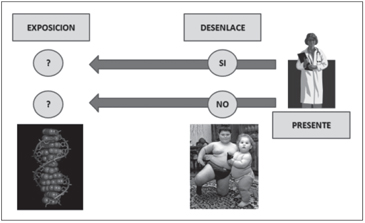 Figura 3. Estudios de casos y controles secuencia temporal.
Figura 3. Estudios de casos y controles secuencia temporal.Tabla 2. Tamaño muestral necesario para detectar asociación significativa (poder 90%, a = 0,001)
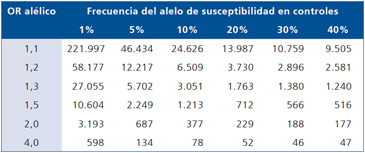 Adaptado de Hatteley A. Lancet; 366: 1315-23.
Adaptado de Hatteley A. Lancet; 366: 1315-23.
Validez interna del estudio
Una vez informados de las características generales de un estudio de asociación genética, podemos iniciar su lectura crítica. La primera etapa es establecer su validez interna a través de comprobar el cumplimiento de los siguientes aspectos:
- Definición del fenotipo: Es la definición estandarizada de
la enfermedad y varía de acuerdo al aspecto de la enfermedad
considerado:
• Predisposición (Desenlaces intermediarios).
• Ocurrencia de la enfermedad.
• Complicaciones de la enfermedad.
• Mortalidad, sobrevida.
• Respuesta a tratamiento.
El fenotipo como variable de respuesta o desenlace puede asumir 2 formas:
• Variable discreta (Cualitativas, dicotómicas): Más relevante clínicamente, pero imprecisiones en la definición.
• Variable continua (Desenlace intermediario): Fáciles de medir con acuciosidad, le confieren mayor poder estadístico al análisis.
- Obtención de los grupos de comparación: En las enfermedades
complejas existen múltiples variables a considerar
al momento de evaluar la asociación entre una variante
genética y un desenlace. En los estudios de casos
y controles se conocen como variables de control y en lo
posible deben ser emparejadas o modeladas. De acuerdo
al efecto que las variables de control tengan en la asociación
se clasifican en confundentes o modificantes de
efecto.
Para que un estudio de asociación genética sea adecuado debe existir una completa descripción de las variables de control.
- Estratificación de la Población: Una de las variables
de control de los estudios de asociación genética es la
composición étnica de la población. Esta variable confundente
e incluso modificadora del efecto de la variante
genética sobre el fenotipo se conoce como estratificación
poblacional. La estratificación poblacional podría generar
una asociación espúrea en 2 situaciones:
• Cuando la probabilidad de desarrollar la enfermedad estudiada varía con la ascendencia.
• Cuando los ancestros tienen diferencias en la frecuencia alélica de polimorfismos no relacionados con la enfermedad estudiada.
Para controlar la estratificación de la población existen 3 procedimientos:
• Uso de poblaciones homogéneas en términos de ancestros (autoreporte).
• Uso de controles extraídos de la familia.
• Uso de controles genómicos de marcadores no ligados (DNA mitocondrial, grupos sanguíneos para segregar amerindios).
- Error de genotipificación: El error es inherente a todos
los sistemas analíticos y puede depender de:
• Problemas con el material biológico (Comparar muestras frescas con almacenadas).
• Problemas con la técnica utilizada.
La magnitud del error de genotipificación varía ampliamente (1 a 30%) y suele minimizarse en GWA. Una manera de apreciar este error es a través de la tasa de recuperación. Muchos autores recomiendan no analizar SNPs con tasa de recuperación inferiores a 90%. Sin embargo, tasas de recuperación altas para los genotipos homocigotos pueden combinarse con tasas de recuperación bajas para heterocigotos.
- Equilibrio de Hardy-Weinberg (EHW): Las frecuencias
alélicas en las poblaciones se mantienen inalteradas de
una generación a otra cuando se cumplen las siguientes
condiciones:
• Falta de mutaciones que afecten la frecuencia alélica.
• Gran descendencia poblacional.
• Apareamiento al azar.
• Baja migración.
• Falta de selección natural.
Las proporciones genotípicas de HW para 2 alelos corresponden al cuadrado del binomio de sus frecuencias alélicas (Figura 4). Las proporciones observadas se comparan con las esperadas mediante prueba de hipótesis (X2 o F de Fischer). Un valor de p < 0,05 es el umbral para detectar un desequilibrio.
Las desviaciones de EHW, respetando las 5 condiciones, sugieren error de genotipificación o estratificación poblacional. En GWA, donde se evalúan miles de asociaciones, hasta un 5% de los SNPs podrían violar EHW.
Un artículo de asociación genética tiene validez interna si:
• Tiene una definición adecuada del fenotipo.
• Tiene una descripción completa de variables de control.
• Tiene algún procedimiento para controlar la estratifi
cación genética.
• Reporta el error de genotipificación.
• Respeta el equilibrio de Hardy-Weiberg.
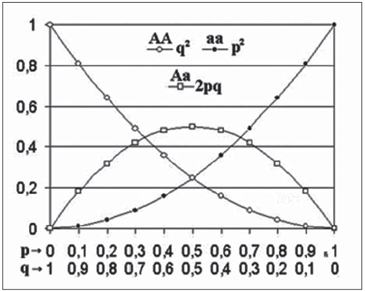 Figura 4. Equilibrio de Hardy-Weiberg.
Figura 4. Equilibrio de Hardy-Weiberg.Análisis de resultados
Una vez que comprobamos que el estudio de asociación
genética cuenta con validez interna podemos analizar sus resultados.
Todo estudio de asociación genética debe considerar
en sus resultados 2 aspectos:
- Comparaciones múltiples: En un estudio asociación genética
entre 100 SNPs y un desenlace clínico determinado,
utilizando un valor p < 0,05, la probabilidad de
asociación espúrea es 99,4%. Este problema afectaría
principalmente a los GWA y podría resolverse por el Método
de Bonferroni que corrige el valor p de acuerdo
al número de comparaciones hechas (0,05/n comparaciones).
En el ejemplo el valor de p sería < 0,0005.
Para GWA que estudian miles de variantes genéticas los
valores de p por Bonferroni serían extremadamente exigentes,
por lo que se ha consensuado un valor p de 5 x
10-8 (Umbral de significación genómica amplia).
- Probabilidad de falso positivo: Cuando revisamos un estudio
de asociación genética con hallazgos positivos y
estamos pensando en replicarlo, existen 2 clases de procedimientos
para evaluar la probabilidad de que se trate
de un falso positivo:
• Método de Benjamini: Utiliza un listado decreciente de valores p de las asociaciones encontradas en el estudio y ajusta cada valor particular de acuerdo a la posición.
• Probabilidad de reporte falso (Wacholder): Establece la probabilidad de una asociación falsa dado el poder del estudio y la OR previa de la asociación.
Un artículo de asociación genética válido, reporta adecuadamente
sus resultados cuando:
• Corrige el valor de p considerando comparaciones
múltiples.
• Reporta la probabilidad de falso positivo.
Validez externa del estudio
En los estudios de asociación genética la tendencia al falso positivo obliga a no considerar seriamente sus resultados hasta que no hayan sido replicadas por estudios independientes. Muchas asociaciones positivas encontradas por estudios pequeños que fueron publicados en el pasado (Sesgo de publicación diferencial), van perdiendo magnitud de efecto con la replicación (Maldición del ganador).
Todo estudio de asociación genética debería establecer si se trata de un estudio inicial o es una replicación en población independiente para el mismo alelo, idéntico fenotipo y dirección de efecto.
Los GWA evalúan SNPs en muestras adicionales de replicación para incrementar su tamaño muestral y alcanzar el umbral de significación genómica amplia. Más allá de los GWA hoy encontramos meta-análisis de estudios de genes candidatos y GWA, que nos permitirían encontrar evidencia de asociaciones genéticas replicadas. El sitio Human Genome Epidemiology Network (HuGE) reúne meta-análisis de estudios de asociación genética y dispone de un navegador para la búsqueda de estudios aislados, GWAs y meta-análisis (http://www.hugenavigator.net/)
Referencias bibliográficas
- Attia J, Ioannidis JPA, Thakkinstian A, McEvoy M, Scott R J, Minelli C, Thompson J, Infante-Rivard C, Guyatt G. 2009. How to use an article about genetic association. Are the results of the study valid? JAMA; 301 (2): 191-197.
- Simundic AM. 2010. Methodological Issues of Genetic Association Studies. Clin Chem Lab Med; 48 (Suppl 1): S115-S118.
- Hatteley A, McCarthy MI. 2005. What makes a good genetic association study? Lancet; 366: 1315-1323.
- NCI-NHGRI. 2007. Working Group on Replication in Association Studies. Replicating genotype-phenotype associations. Nature; 477: 655-660.
- Little J, Higgins JPT, Ioannidis JPA, Moher D, Gagnon F, von Elm E, et al. 2009. STrengthening the REporting of Genetic Association studies (STREGA) - an extensión of the STROBE statement. Eur J Clin Invest 39: 247-266.