Hiperglicemia y diabetes inducidas por esteroides
Mariarlenis Lara1*
Hyperglycemia and steroid-induced diabetes
- Médico internista y endocrinólogo. Unidad de Diabetes, Hospital Barros Luco Trudeau. Santiago, Chile. Docente
del Programa de Medicina Interna de la Facultad de Ciencias Médicas de la Universidad de Santiago de Chile.
Santiago, Chile.
*Correspondencia: Mariarlenis Lara / mariarlenisl@hotmail.com
Dirección: Gran Av. José Miguel Carrera 3122.
Centro de Diagnóstico y Tratamiento (C.D.T.), Unidad de Diabetes. Santiago, Chile.
Financiamiento: El autor declara no tener ninguna fuente de financiamiento.
Recibido: 13-05-2022
Aceptado: 10-06-2022
Resumen: La hiperglicemia y/o diabetes inducida por esteroides, se define como la elevación de la glicemia, causada por la acción de los fármacos glucocorticoideos, sobre el metabolismo de los carbohidratos, y presenta una prevalencia entre un 20% al 50%, en pacientes sin diabetes previa, existiendo mayor riesgo para esta patología en pacientes con diabetes pre-existente, obesidad, uso crónico de esteroides o en dosis altas, entre otros. El diagnóstico se rige por los criterios para diabetes en la mayoría de los casos. No obstante, existen casos en donde la hiperglicemia por esteroides es sub-diagnosticada. Su manejo se basa en el tratamiento farmacológico (antidiabéticos orales, subcutáneos e insulina) y no farmacológico (dieta y ejercicio), tomando en cuenta, el patrón glicémico, peso, edad, co-morbilidades, dosis, tipo y tiempo de uso de los esteroides. La relevancia de conocer como diagnosticar y tratar dicha patología, se debe al riesgo de ingreso hospitalario, de infección, de mala cicatrización y de mortalidad en casos no tratados. En vista del aumento del uso de glucocorticoides en la actualidad, se hace una revisión del abordaje terapéutico de la hiperglicemia y diabetes inducida por esteroides.
Palabras clave: Diabetes; Diabetes esteroidea; Esteroides; Glucocorticoides; Hiperglicemia; Hiperglicemia por esteroides.
Abstract: Hyperglycemia and Steroid-induced Diabetes is defined as the elevation of glycemia caused by the action of glucocorticoid drugs on carbohydrate metabolism, with a prevalence between 20% and 50% in patients without Diabetes. Though, there is a greater risk of this pathology in patients with pre-existing Diabetes, Obesity, chronic use of steroids or in high doses, among others. In most cases, the diagnosis is governed by the criteria of Diabetes; however, there are cases where hyperglycemia Steroid-induced is under-diagnosed. Its management is based on pharmacological treatment (oral and subcutaneous hypoglycemic agents and insulin) and non-pharmacological treatment (diet and exercise), in accordance with the glycemic pattern, weight, age, co-morbidities, dose, type and the duration of the use of steroid. The relevance of knowing how to diagnose and treat this pathology is the risk of hospital admission, infection, poor healing and mortality in untreated cases. In view of the increased use of glucocorticoids nowadays, a review is made about the therapeutic approach to hyperglycemia and steroid-induced Diabetes.
Keywords: Diabetes; Glucocorticoids; Hyperglycemia; Steroid diabetes; Steroid hyperglycemia; Steroids.
Generalidades
Los glucocorticoides, son fármacos ampliamente utilizados en la medicina, para múltiples patologías agudas y crónicas, bien sea, en pacientes hospitalizados o no1,2. En personas con diabetes previa, el uso de glucocorticoides puede inducir la elevación de la glicemia, lo que se define como “hiperglicemia inducida por esteroides” y en personas sin diabetes, esta hiperglicemia se puede definir como “diabetes inducida por esteroides o diabetes esteroidea”, bien sea, que se resuelva o no posterior al retiro del mismo3,4. El efecto de los glucocorticoides suele ser transitorio y reversible, a medida que se reducen sus dosis, desapareciendo así sus efectos adversos, sin embargo, esto no se da en todos los pacientes5.
Durante años, los glucocorticoides han sido la causa principal de hiperglicemia inducida por fármacos, y se ha demostrado que cuando son administrados por vía oral, aumentan el riesgo de diabetes entre un 2% a 11%6,7.
A nivel hospitalario, varios investigadores, han demostrado la presencia de hiperglicemia secundaria al uso de esteroides, en múltiples patologías. Se ha reportado una incidencia entre un 53% a 86% de al menos 1 episodio de hiperglicemia durante el uso de estos fármacos en dosis altas4,5,8,9,10, con una prevalencia entre un 20% a 50%, en pacientes sin diabetes previa11,12. Por tanto, se demuestra que más de la mitad de los pacientes que reciben esteroides a nivel hospitalario o en dosis altas, desarrollan hiperglicemia5,13 y que esta última es más común de lo que parece, en los pacientes no diabéticos hospitalizados, tratados con esteroides en dosis altas10. Estos indicadores toman relevancia al reconocer que, la hiperglicemia se asocia con una mayor estadía hospitalaria, visitas frecuentes a la sala de emergencias, riesgo de ingreso a cuidados intensivos, riesgo de infección, mala cicatrización y mayores tasas de mortalidad hospitalaria5.
Por otro lado, los glucocorticoides también se utilizan como adyuvantes en ciertos regímenes de quimioterapia para prevenir efectos secundarios como náuseas y vómitos, así como, para beneficio terapéutico adicional14; en pacientes trasplantados, es frecuente el uso combinados con fármacos inmunosupresores que, también pueden afectar el metabolismo de la glucosa, presentándose una incidencia de diabetes entre un 2% a 53%, en estos casos15, con una prevalencia entre un 17% a 32%4,12,16. Este uso combinado de fármacos necesarios en las situaciones anteriormente mencionadas, implica que, el equipo de salud debe conocer el manejo del efecto de los glucocorticoides, para así evitar las fluctuaciones en las concentraciones plasmáticas de glucosa, que han mostrado un mayor riesgo de mortalidad cardiovascular16 y de diabetes.
Actualmente, las estrategias para el manejo de la hiperglicemia y la diabetes inducida por esteroides son subóptimas, a causa de pocos estudios disponibles que aborden esta patología. Tatalovic et al., (2019), citan que: “La falta de estudios que informen evidencia de alta calidad, hace difícil proporcionar recomendaciones formales y finales”13, por ello, se hace una revisión práctica del abordaje de la hiperglicemia y la diabetes inducida por esteroides.
Factores de riesgo
Los factores predisponentes para la hiperglicemia inducida por esteroides incluyen una gama de antecedentes y condiciones. A continuación, se especifican en la tabla 1.
Tabla 1. Factores de riesgo para la hiperglicemia y diabetes inducida por esteroides.
- Antecedente familiar de diabetes
- Grupos étnicos
- Edad avanzada
- Diabetes mellitus tipo 1 ó 2 pre-existente
- Antecedente de diabetes gestacional
- Intolerancia a la glucosa
- Sobrepeso u obesidad
- Síndrome de ovario poliquístico
- Historia de hiperglicemia previa por uso de esteroides
- Uso prolongado o crónico de esteroides
- Uso de altas dosis de esteroides (Prednisolona >20 mg, hidrocortisona >50 mg, dexametasona >4 mg)
- Hemoglobina glicosilada A1c (HbA1c) ≥6%
Glucocorticoides
Los glucocorticoides, son hormonas esteroideas producidas en la zona fasciculada de la corteza de las glándulas adrenales, que tienen un papel fundamental en el metabolismo de las proteínas, las grasas y la glucosa17.
Los esteroides de uso terapéutico, se clasifican en glucocorticoides para aquellas moléculas farmacológicas que preferentemente tienen acción similar a las hormonas esteroideas de las glándulas adrenales, sobre los carbohidratos y la inflamación, donde el cortisol es el referente para el cálculo de la potencia glucocorticoidea, así como se han llamado mineralocorticoides los que afectan al sodio (Na) y Potasio (K), donde el referente de la potencia, es la aldosterona18.
Los fármacos tipo glucocorticoides, interfieren en el metabolismo de los hidratos de carbono; la reducción de la captación de la glucosa secundaria a la resistencia a la insulina hepática y periférica1 (disminución de la captación periférica de glucosa), el aumento de la gluconeogénesis hepática16,19, la inhibición de la secreción de la insulina1 y el aumento de las hormonas contrareguladoras (Glucagón)16, pueden provocar hiperglicemia, predominantemente postprandial1. Estos efectos mencionados son dosis-dependientes2,14 y dependen del tipo de glucocorticoides y tiempo de uso.
En el músculo esquelético, pueden inducir resistencia a la insulina, interfiriendo directamente en la cascada de señalización5 (alteran el uso de glucosa a través de defectos posteriores al receptor)16, afectando la disponibilidad de GLUT-45 (disminución de la expresión y migración)16, lo que conlleva a una reducción en la absorción de glucosa y de la síntesis de glucógeno. Se hace notar, que el musculo esquelético es el responsable del 80% del almacenamiento de la glucosa postprandial y representa la mayor reserva de glucógeno corporal dependiente de la acción de la insulina5, de allí la explicación del porqué con el uso de esteroide, las hiperglicemias son predominantemente postprandiales.
Así mismo, los glucocorticoides proporcionan sustratos para el metabolismo del estrés oxidativo, lo que aumenta la lipólisis y la proteólisis; producen elevación de colesterol tipo LDL, disfunción endotelial, activación de la cascada de coagulación, aumento de la producción de citocinas pro-inflamatorias5 y reducen la secreción de la insulina por las células β pancreáticas, porque estas células son vulnerables a la toxicidad por especies de oxígeno (ROS)19 (Tabla 2).
En consecuencia, el uso en dosis elevadas o uso crónico de glucocorticoides, además de hiperglicemia, pueden producir obesidad central, hiperlipidemia hepática, hipertensión arterial, atrofia muscular19, depleción de volumen secundario a la diuresis osmótica y un aumento en la susceptibilidad de infección, sobre todo en paciente con diabetes y mal control metabólico1. Todo ello resulta en la progresión de las enfermedades macrovasculares y en un estado inflamatorio agudo, tanto en paciente con o sin diabetes previa. Otros efectos adversos son: visión borrosa, cambios de humor, insomnio, aumento de peso, osteopenia con osteoporosis posterior, insuficiencia adrenal, acné, adelgazamiento de la piel, dispepsia, necrosis avascular, cataratas, glaucoma de ángulo abierto y psicosis5.
Tabla 2. Mecanismos implicados en la hiperglicemia y diabetes inducida por esteroides.
- Resistencia a la insulina a nivel hepático y periférico
- Disminución de la expresión y migración de GLUT-4
- Gluconeogénesis hepática.
- Reducción de la Glucogenogénesis
- Destrucción de las células pancreáticas (acción proinflamatoria)
- Disfunción de las células β
- Inhibición de la secreción de la insulina
- Aumento de ácidos grasos
- Aumento de las hormonas contrarreguladoras (Glucagón)
- Proporcionan sustratos para el metabolismo del estrés oxidativo
- Aumento de la lipólisis
- Aumento de la proteólisis
Tipos de glucocorticoides
En la actualidad, existen varios tipos de glucocorticoides con diferencias en su farmacocinética y farmacodinamia (Tabla 3); estas diferencias son las que definen su dosificación, temporalidad y uso en diferentes patologías1.
Patrón glicémico por el uso de glucocorticoides
En general, se puede esperar que los niveles de glucosa aumenten entre 4 a 8 horas después de la administración de glucocorticoides orales, y aproximadamente 5 horas después, cuando la administración es endovenosa4. En pacientes que usen glucocorticoides de acción intermedia en una dosis matutina, pueden presentar leve elevación de la glicemia en ayunas con una mayor elevación vespertina, en el caso de glucocorticoides de acción prolongada, la elevación de las glicemias es postprandial, con un descenso en la noche de la misma1.
En continuidad a lo comentado, las concentraciones de glucosa en ayunas en general son típicamente normales cuando los glucocorticoides se administran una vez al día. En este caso, la glucosa aumenta después del desayuno y particularmente después del almuerzo (hiperglicemia postprandial)2,16, con una disminución gradual hacia la normalidad en la noche y la madrugada16, esto es debido a una secreción defectuosa de la insulina postprandial5, especialmente observados en pacientes no diabéticos y en aquellos con diabetes controlada. Este patrón, refleja la reducción del consumo de glucosa en el tejido muscular y adiposo inducido por los glucocorticoides mencionado en párrafos previos. Los preparados de acción intermedia administrados en una sola dosis matutina como se mencionó magnifican este patrón2.
Tabla 3. Tipos de Glucocorticoides.
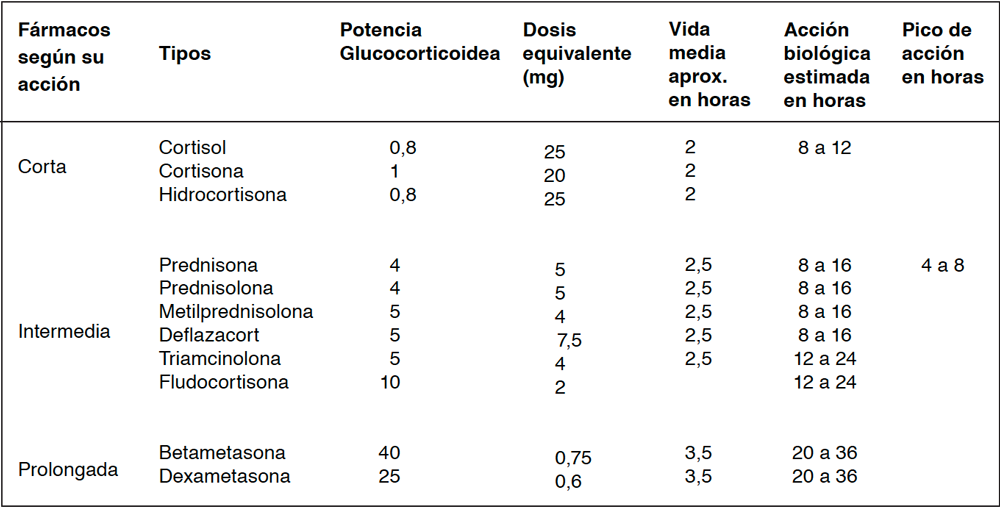 Tomado de: Tamez-Pérez et al.5 Kwon et al.16 y Gómez et al.18
Tomado de: Tamez-Pérez et al.5 Kwon et al.16 y Gómez et al.18
Diagnóstico
El diagnóstico de diabetes inducida por esteroides, se rige por los criterios establecidos por la American Diabetes Association (ADA) (Glicemia sérica en ayunas ≥126 mg/dL y/o glicemia en cualquier momento ≥200 mg/dL con síntomas clásicos de hiperglicemia o glicemia 2 horas post-carga con 75 g de glucosa ≥200 mg/dL y/o HbA1c ≥6,5%, hace el diagnóstico)1,5,20.
No obstante, analizando el patrón de hiperglicemia y el momento donde con mayor frecuencia esta se eleva durante el día, se observa que, con solo el uso de los criterios establecidos por la ADA, existen muchos pacientes con hiperglicemia que no son pesquisados, sobre todo en aquellos casos de tratamientos con glucocorticoides de acción intermedia en mono dosis matutina donde, la glicemia basal se encuentra eventualmente normal y la hiperglicemia se pueden presentar en horas de la tarde.
El test de tolerancia oral a la glucosa, tampoco parece ser idóneo para el diagnóstico de la diabetes inducida por esteroides, porque al medirse solo la glicemia basal y 2 horas post-carga de glucosa, la hiperglicemia predominantemente vespertina en los casos del uso de glucocorticoides, no son medidas2.
La HbA1c puede ser un método adecuado para el diagnóstico en los pacientes con diabetes inducida por esteroides de más de 2 meses de evolución, pero no útil para todas aquellas situaciones en las que es recién iniciado el glucocorticoide. En estos casos, el resultado será un falso negativo, porque el valor de la HbA1c estima la glicemia media de los últimos 3 meses2.
Por tanto, Saigi et al., recomiendan que, para el diagnóstico de diabetes inducida por esteroides, se observen las glicemias postprandiales, especialmente en los pacientes que reciben glucocorticoides de acción intermedia en mono dosis matutina; sugieren que en todo paciente que recibe glucocorticoides en dosis medias-altas, monitorear la glicemia postprandial (mayor sensibilidad para diagnosticar la hiperglicemia inducida por esteroides) y pre-prandial de la cena (menor sensibilidad, pero mejor facilidad de estandarizar) durante los primeros 3 días de iniciado el tratamiento. En los pacientes con diabetes previa o con factores de riesgo, la pesquisa deberá realizarse incluso cuando se indiquen glucocorticoides a dosis bajas2.
Así mismo, Héctor et al., no recomiendan el uso de la glicemia basal, así como la curva de tolerancia a la glucosa como métodos de diagnóstico fiables, porque hay una alta posibilidad de perder algunos de los pacientes hiperglicémicos, y enfatizan que la glicemia postprandial después del almuerzo, ofrece mayor sensibilidad de diagnóstico, especialmente en el uso de glucocorticoides de acción intermedia en monodosis5.
Con respecto a los pacientes hospitalizados independiente de la presencia o no de diabetes previa, se define hiperglicemia hospitalaria una glicemia ≥ (140 mg/dL)10,20, Umpierrez et al., recomiendan que, si existen glicemias en estos valores, solicitar la HbA1C si no se ha realizado alguna en los últimos 3 meses20.
Vigilancia
Varios investigadores recomiendan que cualquier individuo que comience la terapia con glucocorticoides, bien sea, hospitalizado o en atención primaria, debe ser monitoreado durante las siguientes 48 a 72 horas, independientemente de la pre-existencia o no de diabetes1,11,13,14,21 y que en pacientes crónicos que reciben glucocorticoides por un tiempo prolongado, se deberá adicionalmente realizar seguimiento glicémico cada 3-6 meses durante el primer año de su uso14.
Aproximadamente, el 94% de los casos desarrollan hiperglicemia dentro del primer y segundo día del inicio de la terapia con esteroides, por tanto, en pacientes hospitalizados no diabéticos que mantienen niveles de glucosa <140 mg/dL sin requerimientos de insulina durante 24 a 48 horas, se puede suspender el control glicémico5.
Metas glicémicas
En el caso de tratamientos crónicos con glucocorticoides a dosis estables, los objetivos glicémicos y la necesidad de tratamiento farmacológico se basarán en los valores recomendados para la mayoría de pacientes con diabetes mellitus: glicemia preprandial 80-130 mg/dl, post-prandial <180 mg/dl y HbA1c <7%2.
En el caso de paciente hospitalizados, el objetivo de la glicemia pre-prandial es de <140 mg/dl y para una glicemia al azar es de <180 mg/dl, para la mayoría de los pacientes con enfermedad no crítica21.
Tratamiento
El tratamiento de la hiperglicemia inducida por esteroides debe plantearse cuándo los valores de glicemia capilar prepandriales son ≥140 mg/dl y las post-prandiales son ≥200 mg/dl en paciente hospitalizados1 y considerar los criterios de diabetes según la ADA en el caso de no hospitalizados. Para iniciar el tratamiento, se debe considerar el tipo de glucocorticoide indicado, dosificación y temporalidad en su uso.
En general, existen varios tratamientos disponibles, que incluyen, tratamiento farmacológico (antidiabéticos orales y subcutáneos) y no farmacológico (dieta y ejercicio). En cuanto al uso de los antidiabéticos orales, su perfil de acción sobre las glicemias a lo largo del día, no suele coincidir con el patrón de hiperglicemia inducida por los esteroides, por ello, su utilidad queda reservada, en pacientes con glicemias < 200 mg/dl, en pacientes no hospitalizados, pacientes con diabetes controlada solo con medidas no farmacológicas y/o sin diabetes previa, que utilicen bajas dosis de glucocorticoides como tratamiento crónico. En estos casos la terapia puede basarse en cambios del estilo de vida más los antidiabéticos orales, tales como la metformina (contraindicado en pacientes con co-morbilidades asociadas a hipoxia e insuficiencia renal)5, las glinidas (permiten una mínima titulación de dosis, reducen el riesgo de hipoglicemias en la madrugada)2, los inhibidores de la dipeptidil peptidasa-4 (DPP-4) (recomendados por su predominante efecto sobre la glicemia post-prandial y riesgo reducido de hipoglicemia), los inhibidores del cotransportador de sodio y glucosa tipo 2 (SGLT2) (aunque hay algunos efectos adversos no deseados como las micosis genitales, las infecciones del tracto urinario)5 y los agonistas del péptido similar al glucagón tipo 1 (GLP-1) (actualmente hay escasa evidencia de su uso en diabetes esteroidea)3,13,16.
En algunos pacientes que ya estén recibiendo antidiabéticos orales previo al inicio de los glucocorticoides, se puede aumentar las dosis de los mismos o combinarlos temporalmente con otros antidiabéticos o con insulina3.
Las tiazolinedionas y las sulfonilureas, por muchos años fueron recomendadas. En la actualidad, con el primer grupo de fármacos, se ha disminuido su uso por el riesgo y contraindicación en edema macular, hepatotoxicidad, fracturas, cáncer de vejiga o hematuria macroscópica inexplicable y posibles efectos cardiovasculares como la insuficiencia cardiaca3,5; y con el segundo grupo, por el riesgo de hipoglicemia sobre todo en casos con tratamiento esteroideo de acción corta o en monodosis5. Para los demás casos, la insulina es el tratamiento de elección.
Insulina
La nomenclatura de la insulina incluye 3 componentes en los esquemas: insulina basal (inhibe la producción de glucosa hepática durante la noche y entre comidas), insulina prandial (también llamada bolo o de hora de las comidas y promueve la eliminación de glucosa desde el consumo de alimentos) e insulina por dosis de corrección. Este último componente a menudo se confunde con el esquema móvil o deslizante de insulina; la insulina en dosis de corrección se administra habitualmente como una adición a la dosis habitual de la insulina prandial (bolos) como un algoritmo específico basado en la dosis diaria total de insulina o peso del paciente, en cambio, la insulina por esquema móvil es una amalgama de los 3 componentes de la insulina que no tiene ninguna base teórica ni evidencia de efectividad, que se usa por un patrón aprendido o por tradición y asume que todos los pacientes tienen similitud en la sensibilidad o ningún cambio en la misma durante las diferentes etapas de una enfermedad aguda22, por lo tanto, se debe desestimar su uso, a pesar de que en algunos estudios, demostró que, mejora el tiempo en el rango objetivo de glucosa en pre-prandiales13.
En cuanto al tipo de esquema de insulina, ha demostrado que, el esquema de insulina basal-bolo es el más recomendado, independiente del tipo de insulina a utilizar y sobre todo en paciente con diabetes previa, bien sea, en atención ambulatoria de consulta o en hospitalización13,23. Por tanto, el tratamiento con el esquema basal-bolo es más eficaz comparado con el esquema móvil de insulina en el manejo de la hiperglicemia24.
Así mismo, al momento de escoger el tipo de insulina, lo ideal es que su efecto coincida con el perfil de elevación glicémico del tipo de glucocorticoide administrado (insulina NPH para pacientes en tratamiento con prednisolona o insulina glargina o detemir para pacientes con dexametasona)5,13. Por ejemplo, se sugiere administrar insulina basal con NPH nocturna (11 pm), en pacientes con diabetes previa, que presentan hiperglicemias en ayunas en al menos dos mañanas consecutivas, en cambio, si la tendencia de las hiperglicemias es vespertina (secundaria a la administración del esteroide en la mañana) la dosis de insulina NPH se deberá administrarse en horas de la mañana5.
Esta última insulina, puede lograr un buen control de las elevaciones de glicemia vespertinas secundarias al uso de glucocorticoides13, idealmente cuando se usa prednisona o prednisolona vía oral como se mencionó anteriormente, porque esta insulina tiene un perfil de acción similar a estos glucocorticoides16. No obstante, se debe usar con precaución por mayor riesgo de hipoglicemia, si se utiliza en conjunto con insulina en bolos13. Si el uso de esteroides es multidosis, la insulina NPH generalmente no es suficiente para mantener la glicemia, por tanto, se deberá realizar esquema basal-bolo5.
Una vez decidido el tipo de insulina (Tabla 4) que mimetiza el perfil de acción hiperglicemiante de los glucocorticoides (Tabla 3), se deberá decidir el esquema de insulina a utilizar (esquema insulina basal, basal-bolo o basal-bolo más dosis de insulina de corrección) y calcular dosis en base al peso del paciente, el total de calorías consumidas durante las comidas, el patrón de alimentación5 y el factor de sensibilidad. Se recomienda el inicio de la terapia con insulina a una dosis de 0,3 a 0,5 unidades/Kg/día en caso de pacientes hospitalizados16,24 e iniciar a 0,1 UI/kg/día en pacientes de consulta y se va modificando según la respuesta glicémica del mismo5.
Tabla 4. Duración del efecto de las insulinas.
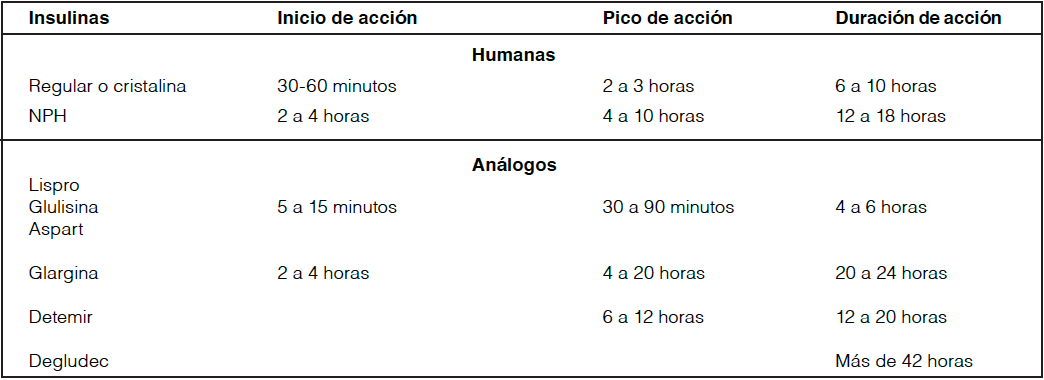
Si se inicia con doble-dosis de glucocorticoides y previamente no recibía insulina, se recomienda administrar 2 dosis de insulina en caso de ser NPH, distribuida en 2/3 predesayuno y 1/3 pre-cena1; si el paciente no logra las metas glicémicas propuestas (en caso de un esquema basal)16 o si el paciente continúa ameritando correcciones pre-prandiales (en caso de que se inició un esquema basal-bolo con insulina por dosis de corrección)5, o en el caso de uso previo de insulina, se deberá aumentar la dosis de esta cada 24 a 48 horas3, tomando en cuenta el patrón glicémico y cantidad total de insulina por dosis de corrección utilizada según sea el caso y repetir ajustes hasta lograr las metas glicémicas16.
Según Kwon et al., en los casos de esquema basal-bolo con insulina por dosis de corrección, plantean agregar del 50% al 100% de la dosis de insulina de corrección requerida en las últimas 24 horas e incrementar la escala de corrección16. Héctor et al., indican que en caso de requerir corrección de la hiperglicemia pre-prandial se puede realizar el cálculo según el valor de glicemia a 0,04 UI/kg/dosis por comida, si las glicemias están entre 200-300 mg/dl y a 0.08 UI/kg/ dosis por comida, si están por encima de 300 mg/dL5. Por último, Saigi et al., sugieren aumentar en un 20-30% de la dosis habitual predominando el aumento en la dosis que coincide con la administración del glucocorticoide1. Según sea la manera que se elija corregir, lo importante es realizar el aumento de la insulina basal y ajustar los bolos y la escala de insulina por dosis de corrección, según el adicional de insulina requerido por el paciente en las últimas 24 horas para prevenir la variabilidad glicémica.
En pacientes hospitalizados que, a pesar de tener un esquema basal-bolo, presentan hiperglicemia severa (>400 mg/dl) o persistente y reciben altas dosis de esteroides o por vía endovenosa en los que los requerimientos de insulina son difíciles de predecir, se recomienda iniciar bomba de infusión de insulina5. La bomba se retira una vez lograda glicemia <200 mg/dl, donde para el cambio a vía subcutánea se realiza en pre-comida, administrando la dosis de insulina subcutánea correspondiente y se espera 2 horas para la suspensión de la bomba de infusión. El cálculo de la dosis de insulina subcutánea diaria, se recomienda estimar de acuerdo con la dosis endovenosa de las ultimas 4 a 8 horas, administrándose el 80% de la dosis total si se mantiene estable, o el 50% si se inicia descenso de dosis de los glucocorticoides en las siguientes 24 horas o si existe riesgo de hipoglicemia1.
Por último, los pacientes, familiares y cuidadores deben ser instruidos sobre el manejo de la diabetes a la hora del alta hospitalaria. Las instrucciones deben incluir monitoreo de la glicemia, identificación y manejo de la hipoglicemia y acudir a los controles para vigilar el ajuste de los medicamentos que pueden influir en las glicemias como es el caso de los glucocorticoides11.
Recomendaciones finales
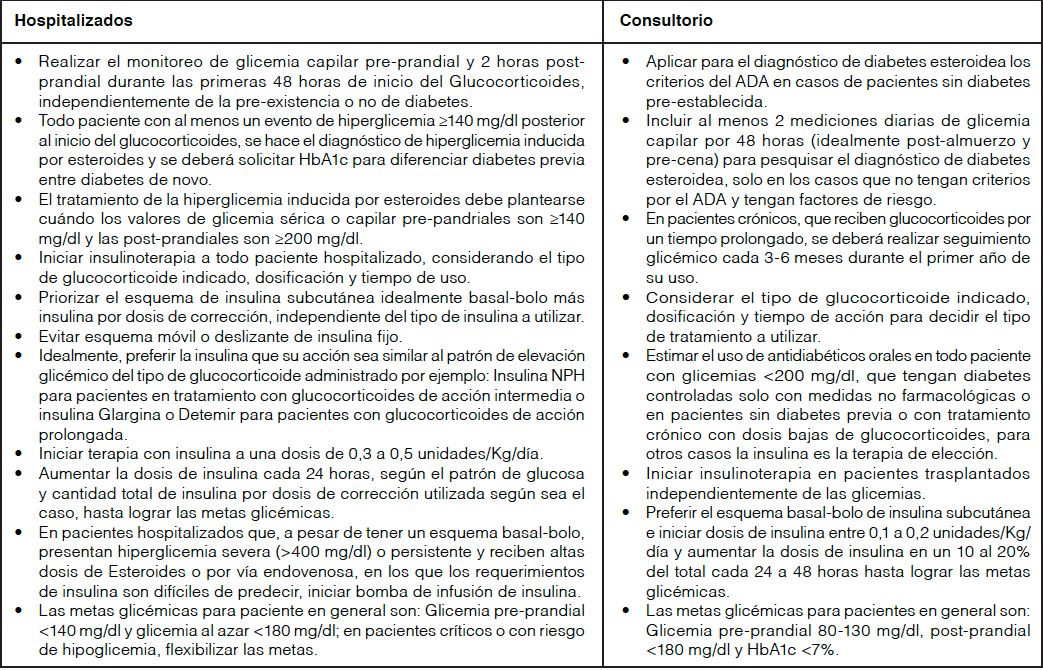
A modo de resumen, se comenta en la tabla 5, lo más
relevante del manejo de la hiperglicemia y la diabetes inducida
por esteroides.
Referencias
- Saigí I, Pérez A. Manejo de la hiperglucemia inducida por corticoides. Rev Clin Esp. 2010; 210(8): 397-403.
- Saigí I. Pérez A. Hiperglucemia inducida por glucocorticoides. Semin Fund Esp Reumatol. 2011; 12(3): 83-90.
- Roberts A, James J, Dhatariya K. Management of hyperglycaemia and steroid (glucocorticoid) therapy: a guideline from the Joint British Diabetes Societies (JBDS) for Inpatient Care group. Diabet Med. 2018 Aug; 35(8): 1011-1017. doi: 10.1111/dme.13675. PMID: 30152586.
- Suh S, Park MK. Glucocorticoid-Induced Diabetes Mellitus: An Important but Overlooked Problem. Endocrinol Metab (Seoul). 2017 Jun; 32(2): 180- 189. doi: 10.3803/EnM.2017.32.2.180.
- Tamez-Pérez HE, Quintanilla-Flores DL, Rodríguez-Gutiérrez R, González- González JG, Tamez-Peña AL. Steroid hyperglycemia: Prevalence, early detection and therapeutic recommendations: A narrative review. World J Diabetes. 2015 Jul 25; 6(8): 1073-1081. doi: 10.4239/wjd.v6.i8.1073.
- Gulliford MC, Charlton J, Latinovic R. Risk of Diabetes associated with prescribed glucocorticoids in a large population. Diabetes Care. 2006 Dec; 29(12): 2728-2729. doi: 10.2337/dc06-1499. PMID: 17130214.
- Blackburn D, Hux J, Mamdani M. Quantification of the risk of corticosteroidinduced Diabetes Mellitus among the elderly. J Gen Intern Med. 2002; 17: 717-720.
- Burt MG, Roberts GW, Aguilar-Loza NR, Frith P, Stranks SN. Continuous monitoring of circadian glycemic patterns in patients receiving prednisolone for COPD. J Clin Endocrinol Metab. 2011 Jun; 96(6): 1789-1796. doi: 10.1210/jc.2010-2729.
- Donihi AC, Raval D, Saul M, Korytkowski MT, DeVita MA. Prevalence and predictors of corticosteroid-related hyperglycemia in hospitalized patients. Endocr Pract. 2006; 12: 358-362.
- Fong AC, Cheung NW. The high incidence of steroid-induced hyperglycaemia in hospital. Diabetes Res Clin Pract. 2013 Mar; 99(3): 277-280. doi: 10.1016/j. diabres.2012.12.023.
- Houlden R, Capes S, Clement M, Miller D. In-hospital Management of Diabetes. Canadian Diabetes Association Clinical Practice Guidelines Expert Committee. Can J Diabetes. 2013; 37: S77eS8.
- Liu XX, Zhu XM, Miao Q, Ye HY, Zhang ZY, Li YM. Hyperglycemia induced by glucocorticoids in nondiabetic patients: A meta-analysis. Ann Nutr Metab. 2014; 65(4): 324-332. doi: 10.1159/000365892
- Tatalovic M, Lehmann R, Cheetham M, Nowak A, Battegay E, Rampini SK. Management of hyperglycaemia in persons with non-insulin-dependent type 2 Diabetes Mellitus who are started on systemic glucocorticoid therapy: A systematic review. BMJ Open 2019; 9: e028914. doi:10.1136/ bmjopen-2019-028914.
- Rowbottom L, Stinson J, McDonald R, Emmenegger U, Cheng S, Lowe J, et al. Retrospective review of the incidence of monitoring blood glucose levels in patients receiving corticosteroids with systemic anti-cancer therapy. Ann Palliat Med. 2015; 4(2): 70-77. doi: 10.3978/j.issn.2224-5820.2015.04.07.
- Perez A, Jansen-Chaparro S, Saigi I, Bernal-Lopez MR, Miñambres I, Gomez-Huelgas R. Glucocorticoid-induced hyperglycemia. J Diabetes. 2014 Jan; 6(1): 9-20. doi: 10.1111/1753-0407.12090. Epub 2013 Oct 29. PMID: 24103089.
- Kwon S, Hermayer KL, Hermayer K. Glucocorticoid-induced hyperglycemia. Am J Med Sci. 2013 Apr; 345(4): 274-277. doi: 10.1097/MAJ.0b013e31828a6a01. PMID: 23531958.
- Chourpiliadis C, Aeddula NR. Physiology, Glucocorticoids. 2021 Jul 22. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 Jan. PMID: 32809732.
- Gómez-Ordóñez S, Gutiérrez-Álvarez Á, Valenzuela-Plata E. Corticoides: 60 años después, una asignatura pendiente Rev. Cienc. Salud. Bogotá (Colombia). 2007 Sep; 5 (3): 58-69.
- Niu L, Chen Q, Hua C, Geng Y, Cai L, Tao S. et al. Effects of chronic dexamethasone administration on hyperglycemia and insulin release in goats. Journal of Animal Science and Biotechnology. 2018; 9: 26. https:// doi.org/10.1186/s40104-018-0242-4.
- American Diabetes Association; Standards of Medical Care in Diabetes-2022 Abridged for Primary Care Providers. Clin Diabetes. 2022 January 1; 40 (1): 10-38. https://doi.org/10.2337/cd22-as01
- Umpierrez GE, Hellman R, Korytkowski MT, Kosiborod M, Maynard GA, Montori VM, et al. Endocrine Society. Management of hyperglycemia in hospitalized patients in non-critical care setting: An endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2012 Jan; 97(1): 16-38. doi: 10.1210/jc.2011-2098. PMID: 22223765.
- Hirsch IB. Sliding Scale Insulin-Time to Stop Sliding. JAMA. 2009; 301(2): 213-214. doi:10.1001/jama.2008.943.
- Roberts GW, Aguilar-Loza N, Esterman A, Burt MG, Stranks SN. Basalbolus insulin versus sliding-scale insulin for inpatient glycaemic control: A clinical practice comparison. Med J Aust. 2012 Mar 5; 196(4): 266-269. doi: 10.5694/mja11.10853. PMID: 22409694
- Gosmanov AR, Goorha S, Stelts S, Peng L, Umpierrez GE. Management of hyperglycemia in Diabetic patients with hematologic malignancies during dexamethasone therapy. Endocr Pract. 2013 Mar-Apr; 19(2): 231-235. doi: 10.4158/EP12256.OR. PMID: 23337144.