Modulación de marcadores de inflamación y estrés oxidativo en pacientes con diabetes tipo 1 y sobrepeso que participan en un programa de cambio de estilo de vida
Alejandra Cicchitti P1, Isabel Quesada2, Jimena Cejas2, Celina Bertona A1, Joaquín González V1, Walter Rosales R1, Guillermo Esteves M1, Gabriel Minuchín B1, Martín Rodríguez G3 y Claudia Castro2.
Modulation of Inflammatory and oxidative stress markers in overweight type 1 Diabetes patients participating in a lifestyle change program
1Hospital Universitario, Universidad Nacional de Cuyo. Mendoza, Argentina.
2. Área de Química Biológica, Facultad de Ciencias Médicas-Universidad Nacional de Cuyo y Laboratorio de Biología Vascular, IMBECUCONICET. Mendoza, Argentina
3. Instituto de Endocrinología, Metabolismo y Nutrición, Facultad de Ciencias Médicas- Universidad Nacional de Cuyo. Mendoza, Argentina.
Correspondencia:
Claudia Castro
Facultad de Ciencias Médicas, Universidad
Nacional de Cuyo.
Avda. Libertador 80, 5500 Mendoza,
Argentina
Teléfono: 54 261 4135000 ext 2721
Correo: ccastro@fcm.uncu.edu.ar
Recibido: 26-06-2018
Aceptado: 05-08-2018
Abstract: Introduction: Reduction in the expression of inflammatory markers and oxidative stress associated with exercise will protect against cardiovascular complications in Diabetes Mellitus (DM). Aim: The aim of this study was evaluated cardiovascular fitness (VO2Max), interleukin-6 (IL-6), monocyte chemo-attractant protein 1 (MCP-1) and serum lipid peroxidation (TBARS) in overweight patients with Type-1 diabetes (T1DM) participating in a lifestyle-change program. Results: 20 T1DM overweight patients (43.3 ± 13.8 years), with BMI= 29.6 ± 3.5 kg/m2, initial HbA1c 7.9 ± 0.91% and treated with multiple insulin injections, were included in this work. The lifestyle-change program consisted of: a) walking 10,000 steps/day, b) sequence of exercises of 24 minutes, 3-5 times/week, c) ¨healthy-plate¨ (and counting carbohydrates, and d) prandial insulin as blood-glucose levels. VO2max, HbA1c, TBARS, IL6, MCP-1 were determined before starting the lifestyle-change program. Six months of adherence later, participants showed an average number of steps of 8242 ± 1834, a significant increase in VO2max, (33.4 ±1.3 vs 36.2 ±1.5 ml.Kg-1.min-1 p= 0.008), a significant decrease in serum MCP-1 (314 ±42 vs 235 ±43 MFI p= 0.02), and less TBARS (3.01 ±0.44 vs 2.12 ±0.22 μmol/mL p= 0.015). IL-6 and HbA1c showed no significant decrease. Conclusion: Our results showed that a 6-month systemized and simple exercise plan improves cardiorespiratory fitness (VO2max), and reduces both circulating oxidative stress and inflammation markers in overweight patients with T1DM.
Key Words: Diabetes; Exercise; Lipid Peroxidation; Inflammation.
Resumen: Introducción: La reducción en la expresión de marcadores inflamatorios
y de estrés oxidativo asociado con el ejercicio podría proteger contra las complicaciones
cardiovasculares de la diabetes mellitus (DM). Objetivo: El objetivo de este
estudio fue evaluar en pacientes con DM tipo1 (DMT1) y sobrepeso, la capacidad
cardiorespiratoria (VO2max), la expresión sérica de marcadores inflamatorios (IL-6
y MCP-1) y la peroxidación lipídica sérica (TBARS), luego de participar por 6 meses
de un programa de cambios de estilo de vida. Resultados: Veinte pacientes adultos
(43.3 ± 13.8 años), de ambos sexos, con un Índice de Masa Corporal de 29.6 ± 3.5
kg/m2, HbA1c inicial de 7,9% ± 0,91, en tratamiento con inyecciones múltiples de
insulina participaron del estudio. Se indicó: 1) caminar 10.000 pasos/día, 2) realizar
en domicilio una secuencia de ejercicios de 20 minutos, 3-5 veces/semana, 3)
plato saludable (consumo de 1 fruta antes de las 3 comidas principales), 4) Insulina
prandial según glucemia y conteo de carbohidratos. Se registraron parámetros
antropométricos, presión arterial, se determinó VO2max, y se midieron los niveles
séricos de HbA1c, IL6, MCP-1 y TBARs. Luego de seis meses, los participantes
alcanzaron un número promedio de pasos de 8242 ± 1834 y mostraron un aumento significativo en VO2max, (33.4 ±1.3 vs 36.2 ±1.5 ml.Kg-1.min-1 p= 0.008). Además,
se encontró una disminución significativa de MCP-1 (314 ±42 vs 235 ±43 MFI p=
0.02) y TBARs (3.01 ±0.44 vs 2.12 ±0.22 μmol/mL p= 0.015) en comparación con
el día 0. No se observaron modificaciones en los niveles de IL-6 y HbA1c. Conclusión:
Nuestros resultados demuestran que el ejercicio, implementado como un plan
accesible y acompañado, es adecuado para reducir los riesgos de inflamación y
estado pro-oxidativo en pacientes con DM tipo1.
Palabras Clave: Diabetes; Ejercicio, Inflamación; Estrés Oxidativo.
La diabetes mellitus (DM) está estrechamente relacionada con las enfermedades cardiovasculares (ECV)1 y los pacientes con DM tipo 1 (DMT1) tienen mayor riesgo de complicaciones cardiovasculares en comparación con la población sana2. La hiperglucemia, el estrés oxidativo y la inflamación son factores claves que contribuyen a la ECV, que a su vez es más frecuente y ocurre más temprano en pacientes con diabetes que en individuos con normoglucemia3,4. La diabetes y el sobrepeso están asociados con la inflamación sistémica persistente5-8 y, contrariamente a lo que ocurria con anterioridad, la prevalencia de sobrepeso en pacientes con DMT1 es ahora similar a la de la población general9. La obesidad aumenta el riesgo de comorbilidades en personas con DMT1, especialmente las enfermedades micro y macrovasculares8. Por lo tanto, son necesarias estrategias para lograr el control de peso en pacientes con DMT1.
La inflamación es mayor en pacientes con DM que en pacientes sin diabetes y, en particular, en individuos con DMT110. Estudios recientes muestran elevaciones de proteína C reactiva (PCR) en niños con diagnóstico reciente de DMT111 y un aumento significativo en los niveles de diferentes citoquinas (IL-1β, IL-6, TNF-α, GM-CSF) en pacientes jóvenes con DMT112. El papel del estrés oxidativo y la inflamación en la progresión de las complicaciones vasculares de la DM está bien establecido, y los mecanismos por los cuales la inflamación y el estrés oxidativo son mayores en personas con DMT1 se relacionan con la hiperglucemia, la hipoglucemia, la distribución alterada de la grasa y el aumento de adipocinas13-17.
El ejercicio regular reduce la resistencia a la insulina y el riesgo cardiovascular al interferir con los mecanismos fisiopatológicos de la ECV a diferentes niveles. El estudio LOOK AHEAD, demostró una reducción significativa de CRP en personas con DM después de un año de intervención en el estilo de vida18. Si bien el ejercicio produce una respuesta inflamatoria a corto plazo, con aumento del estrés oxidativo y mayores niveles de PCR, esta breve respuesta proinflamatoria es seguida por un efecto antiinflamatorio a largo plazo19. No hay duda de que el ejercicio es necesario o, al menos, cumple un propósito funcional inmediato, pero el inconveniente central de realizar ejercicio es la mala adherencia, lo cual constituye uno de los comportamientos humanos más problemáticos20,21,22.
El objetivo de este estudio fue evaluar la capacidad cardiorespiratoria (VO2max), los niveles séricos de interleuquina 6 (IL-6), proteína quimioatractiva-1 de monocitos (MCP-1) y peroxidación lipídica (TBARS), en pacientes con DMT1 y sobrepeso antes y después de 6 meses de participar en un programa de cambio de estilo de vida, que incluía un plan de ejercicio simple.
Sujetos, Material y Métodos
Todos los procedimientos se realizaron de acuerdo con los estándares éticos del comité responsable de experimentación humana (Comité de Ética e Investigación del Hospital Universitario) y con la Declaración de Helsinki de 1964, revisada en 2013. Los pacientes que aceptaron participar en el estudio asisten al Hospital Universitario de Mendoza, Argentina y todos firmaron un consentimiento. Veinte pacientes adultos con DMT1, con un índice de masa corporal (IMC)> 25 kg/m2, con múltiples inyecciones diarias de insulina participaron en el programa. Se excluyeron los pacientes con hipertensión no controlada (>160/100 mmHg), insuficiencia cardíaca, neuropatía diabética grave o retinopatía diabética que requieren tratamiento. En una visita inicial, se registró una evaluación clínica completa, medición de peso y altura con ropa ligera y sin calzado, circunferencia de la cintura a nivel del ombligo y mediciones de la presión arterial.
Programa de cambio de estilo de vida (LSCP)
Los participantes fueron invitados a participar en un simple LSCP, que consistió en: 1) caminar 10,000 pasos por día (cada participante recibió un podómetro) y realizar una serie de ejercicios aeróbicos y de fuerza, sin supervisión en el hogar, durante aproximadamente 20 minutos, 3-5 veces / semana. 2) El consumo de 1 fruta antes de las 3 comidas principales y un plato saludable que consiste en la mitad del plato con vegetales, un cuarto del plato con proteínas y un cuarto con carbohidratos, sugerido según la recomendación de la Asociación Americana de Diabetes (ADA). 3) Uso de insulina basal y ajuste de insulina prandial según glucemia y conteo de hidratos de carbono.
Se programaron visitas mensuales para el ajuste de la dosis y para el control clínico.
Medida de la capacidad cardiorrespiratoria (VO2max)
La VO2max expresa el consumo de O2 al máximo esfuerzo.
En una visita inicial, VO2 se estimó mediante Prueba de Step Test del American College Sport Medicine (ACSM) según Heydari et al23. Después de 6 meses, la estimación se realizó nuevamente.
Determinaciones bioquímicas
Se tomaron muestras de sangre (~10 ml) de la vena antecubital del brazo utilizando una aguja desechable de calibre 20 con un soporte Vacutainer, de los participantes sentados, después de 12 horas de ayuno. Se utilizó una alícuota de sangre completa para determinar la hemoglobina glucosilada (HbA1c), el resto se centrifugó sin anticoagulante a 3000 g durante 15 minutos, y el sobrenadante (suero) se separó en los volúmenes requeridos para cada determinación y se almacenó a -70°C hasta la realización de las determinaciones bioquímicas.
El día 0 y después de 6 meses de participar en el programa, la HbA1c se determinó mediante DCA 2000, IL-6 y MCP-1se determinaron mediante citometría de flujo utilizando el kit bead-flex de BD-Bioscience y las sustancias reactivas al ácido tiobarbitúrico (TBARS) se midieron espectrofotométricamente (530 nm) después de la adición de ácido tiobarbitúrico como se describió previamente24.
Análisis estadístico
Todos los análisis se realizaron utilizando GraphPad Prism versión 6.0 (GraphPad Software, CA, EE. UU) y el paquete estadístico SPSS (Versión 20.0; SPSS, Chicago, IL). Se utilizó prueba t de Student para comparar grupos con variables continuas, y la prueba de rango con signo de Wilcoxon se usó como una prueba estadística no paramétrica, cuando se compararon dos muestras relacionadas, independientemente de si los rangos de la media poblacional eran diferentes o no.
El valor de p menor que 0.05 se consideró significativo.
Resultados
Las características de los pacientes antes y después de participar en este estudio se presentan en la Tabla 1. Después de 6 meses de iniciación del programa LSPC, los participantes alcanzaron un número promedio de pasos por mes de 8,242 ± 1,834 y no se encontraron diferencias estadísticamente significativas en el peso (P= 0.83), circunferencia de la cintura (P= 0.61) y HbA1c (7.9% ± 0.9, vs 7.6% ± 0.8). Es sabido que la actividad física regular aumenta el consumo máximo de oxígeno y posteriormente, aumenta la condición física. En este estudio la capacidad cardiorrespiratoria (VOmax) mostró una mejora significativa después de 6 meses de adherencia al LSCP en todos los participantes (Figura 1).
Dado que el ejercicio físico es un importante modulador de citoquinas y quimiocinas, se determinaron marcadores inflamatorios, antes y después de los 6 meses de adherencia al programa. Se encontró que, comparado con el estado basal, el nivel de proteína quimiotáctica de monocitos soluble (MCP-1) disminuía significativamente (P<0.05), mientras que no se observó una variación estadísticamente significativa en los niveles de Il-6 (Figura 2).
| Antes (n= 20) |
Después (n= 20) |
Pvalue | |
| Años de edad | 43.3 ± 13.8 | ||
| Duración de la enfermedad (años) | 20.5 ± 11.5 | ||
| Género | 11♂ / 9 ♀ | ||
| Peso (kg) | 85.5 ± 2.7 | 84.6 ± 2.8 | 0.83 |
| Índice de masa corporal (kg/m2) | 29.6 ± 0.8 | 29.3 ± 0.8 | 0.77 |
| Circunferencia de la cintura (cm) | 100.4 ± 2.1 | 98.78 ± 2.3 | 0.62 |
| Hba1c (%) | 7.9 ± 0.9 | 7.6 ± 0.8 | 0.33 |
| PA sistólica (mm HG) | 127.0 ± 2.4 | 124.8 ± 2.67 | 0.54 |
| PA diastólica (mm HG) | 76.0 ± 1.9 | 78.1 ± 1.9 | 0.43 |
| Hipertensión | 3 / 20 | 3 / 20 | |
| Medicación antihipertensiva | 9 / 20 | 9 / 20 |
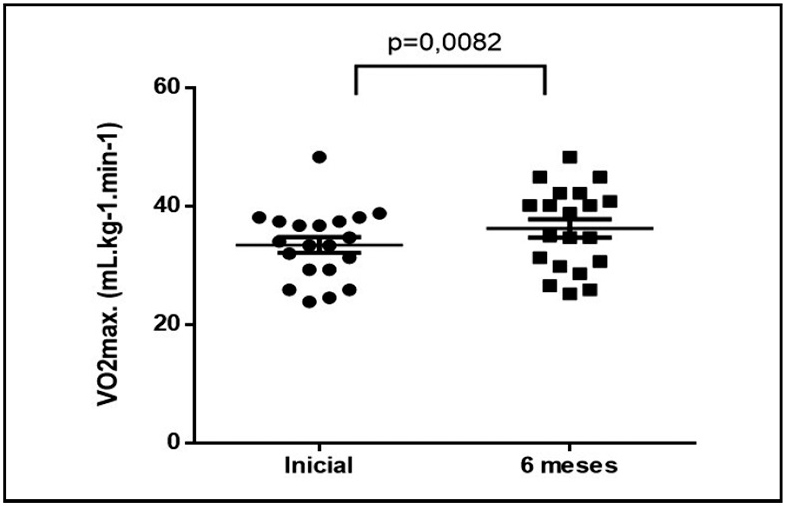 Figura 1. Evaluación del consumo máximo de oxígeno (VO2Máx) estimado por Step Test del American College of Sport Medicine. Los datos
representan Promedio ± SEM. Las diferencias entre el día cero y después de 6 meses de adherencia al programa de cambios de estilo de vida
se calcularon utilizando la prueba t de Student y Wilcoxon. P< 0.01 versus basal.
Figura 1. Evaluación del consumo máximo de oxígeno (VO2Máx) estimado por Step Test del American College of Sport Medicine. Los datos
representan Promedio ± SEM. Las diferencias entre el día cero y después de 6 meses de adherencia al programa de cambios de estilo de vida
se calcularon utilizando la prueba t de Student y Wilcoxon. P< 0.01 versus basal. 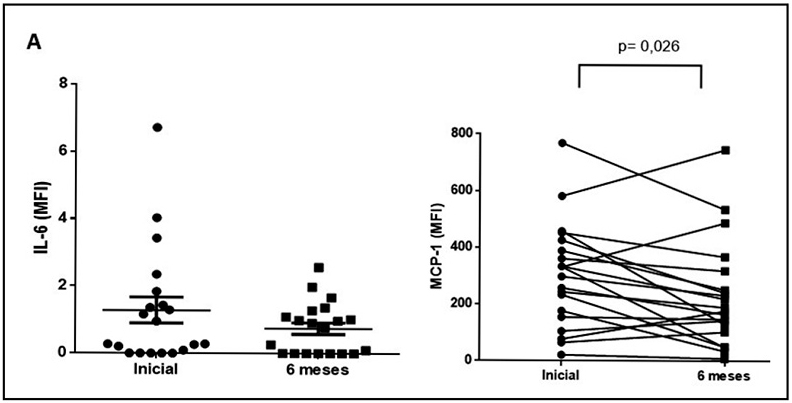 Figura 2. Determinación de los niveles séricos de A) Interleuquina-6 (IL-6); y B) proteína quimiotáctica de monocito-1 (MCP-1) en pacientes
con DMT1 y sobrepeso. Los datos representan el promedio ± SEM de la intensidad de fluorescencia media (IMF). Las diferencias entre el día
cero y después de 6 meses de adherencia al programa de cambios de estilo de vida se calcularon usando una prueba t de Student y Wilcoxon.
P <0.05 versus basal.
Figura 2. Determinación de los niveles séricos de A) Interleuquina-6 (IL-6); y B) proteína quimiotáctica de monocito-1 (MCP-1) en pacientes
con DMT1 y sobrepeso. Los datos representan el promedio ± SEM de la intensidad de fluorescencia media (IMF). Las diferencias entre el día
cero y después de 6 meses de adherencia al programa de cambios de estilo de vida se calcularon usando una prueba t de Student y Wilcoxon.
P <0.05 versus basal. Con el fin de determinar el estres oxidativo circulante en los participantes del estudio, se midieron los TBARS en suero, y se encontró que la peroxidación de lípidos disminuía significativamente después de 6 meses de adherencia al programa (P< 0,01)(Figura 3).
El ejercicio mejora el rendimiento y los parámetros bioquímicos en promedio, sin embargo, este estudio mostró una variabilidad interindividual. Cuando se examinó el cambio de peso en la semana 24, los participantes pudieron clasificarse en dos grupos (respondedores y no respondedores) en función de su cambio de peso calculado, según lo descrito por King y col4. Los pacientes “no respondedores” (n= 9) disminuyeron ≤ 1 kg o aumentaron de peso en comparación con los participantes restantes (“respondedores”, n= 11) que disminuyeron ≥1 kg. Comparando ambos grupos, aparecieron respuestas similares, con la excepción del grupo de respondedores que muestra una mayor disminución tanto en MCP-1 como en TBARS y un mayor aumento en VO2max (Figura 4).
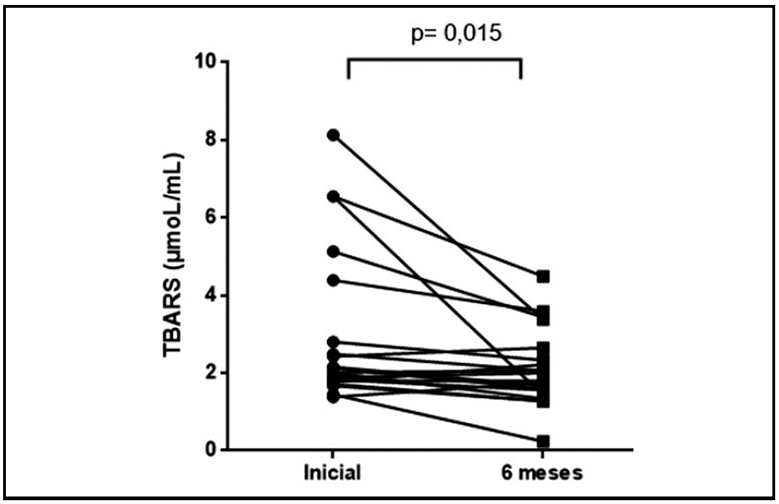 Figura 3. Determinación de los niveles plasmáticos de TBARS en pacientes con DMT1 y sobrepeso. La peroxidación lipídica se determinó
mediante la cuantificación de productos reactivos con ácido tiobarbitúrico (TBARS). Los datos representan Promedio ± SEM. Las diferencias
entre el día cero y después de 6 meses de adherencia al programa de cambios de estilo de vida se calcularon usando una prueba t de Student
y Wilcoxon. P<0.02 versus basal
Figura 3. Determinación de los niveles plasmáticos de TBARS en pacientes con DMT1 y sobrepeso. La peroxidación lipídica se determinó
mediante la cuantificación de productos reactivos con ácido tiobarbitúrico (TBARS). Los datos representan Promedio ± SEM. Las diferencias
entre el día cero y después de 6 meses de adherencia al programa de cambios de estilo de vida se calcularon usando una prueba t de Student
y Wilcoxon. P<0.02 versus basal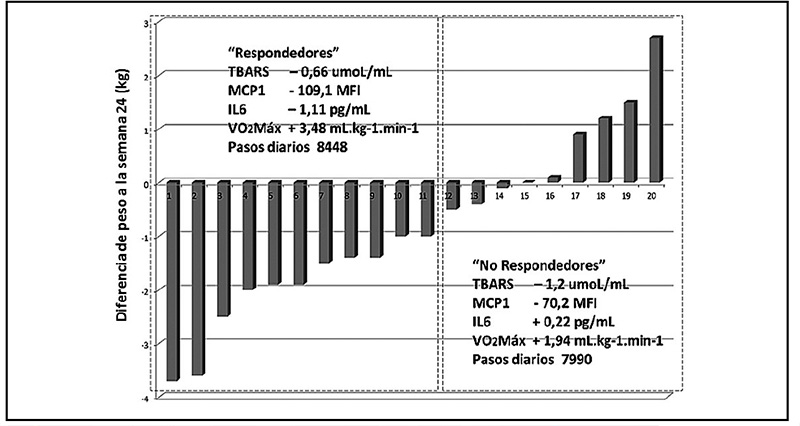 Figura 4. Evaluación de la respuesta al Programa de Cambios en el Estilo de Vida de acuerdo con los cambios en el peso corporal (kg) después de 24 semanas. Los insertos muestran los cambios en la peroxidación de lípidos (TBARS); marcadores inflamatorios (MCP-1 e IL-6) y VO2max después de 24 semanas de ejercicio supervisado en respondedores (n= 11) y no respondedores (n= 9).
Figura 4. Evaluación de la respuesta al Programa de Cambios en el Estilo de Vida de acuerdo con los cambios en el peso corporal (kg) después de 24 semanas. Los insertos muestran los cambios en la peroxidación de lípidos (TBARS); marcadores inflamatorios (MCP-1 e IL-6) y VO2max después de 24 semanas de ejercicio supervisado en respondedores (n= 11) y no respondedores (n= 9).Discusión
El presente estudio evaluó los efectos de un plan de cambio de estilo de vida simple en pacientes con DMT1 y sobrepeso. Como la obesidad y la diabetes se asocian con un aumento de la inflamación y el estrés oxidativo25, el estudio se centró en examinar los marcadores inflamatorios y la peroxidación lipídica sérica. El estudio EURODIAB mostró una asociación inversa en pacientes con DMT1 entre la mortalidad por todas las causas y la actividad física en ambos sexos26. Un estudio transversal con 18.028 adultos con DMT1 mostró una asociación inversa entre actividad física y HbA1c, microalbuminuria y retinopatía, y el grupo con mayor actividad física mostró un mejor perfil de factores de riesgo (presión arterial, lípidos, IMC)27. Los estudios epidemiológicos han demostrado que cada 3,5 ml/Kg-1/min-1 de aumento en el VO2max, expresado como el consumo de O2 al máximo esfuerzo, se alcanza una reducción del 23% en la mortalidad por todas las causas en las poblaciones con DM28. En este estudio, después de 6 meses de adherencia al programa, la aptitud cardiorrespiratoria medida por la captación máxima de oxígeno (VO2max) aumentó en todos los participantes.
En las enfermedades crónicas como la DM, las respuestas agudas y crónicas al ejercicio muestran diferentes respuestas inflamatorias, exageradas después del ejercicio agudo y una respuesta antiinflamatoria menos crónica29. Aunque la ADA considera la inflamación como uno de los principales determinantes de ECV en personas con DMT1, con igual magnitud al tabaquismo, menor magnitud con hipertensión, microalbuminuria y control glucémico, pero de mayor magnitud al colesterol LDL y al bajo HDL-colesterol30, la escasa información sobre el impacto del ejercicio regular sobre la inflamación es sorprendente.
Se ha informado que la IL-6 en plasma aumenta con el ejercicio moderado agudo y tiende a descender por debajo del valor inicial con ejercicio moderado regular, lo que indica que el ejercicio moderado regular tiene efectos beneficiosos(31). Aquí, los niveles plasmáticos de IL-6 disminuyeron levemente y la expresión circulante de MCP-1 se redujo significativamente después de 6 meses de ejercicio. MCP-1 participa en la patogénesis de varias enfermedades caracterizadas por el infiltrado de monocitos como la psoriasis, la artritis reumatoide y la aterosclerosis32. La MCP-1 disminuye significativamente las señales de captación de glucosa por parte del músculo, lo que le confiere un papel importante además de su participación en la inflamación33. Nuestros resultados pueden re- enfatizar el papel prominente de la quimiocina en el control de las complicaciones asociadas a la DMT1.
Existen cada vez más pruebas de que el exceso de generación de especies reactivas del oxígeno, en gran parte debido a la hiperglucemia, causa estrés oxidativo en diferentes tejidos34. El estrés oxidativo es el resultado de un aumento en la producción de radicales libres, una disminución de las defensas antioxidantes endógenas, o ambas, que conduce al daño oxidativo de las macromoléculas celulares, como los lípidos, las proteínas y el ADN35. Esta reportado que el aumento de la peroxidación lipídica en DMT1 disminuye como resultado del tratamiento intensivo con insulina36. En este estudio, después de 6 meses de un programa de cambio de estilo de vida no complejo, los pacientes con DMT1 mostraron una disminución de los TBARS sericos en comparación con el valor inicial, lo que sugiere un efecto beneficioso de disminución de la peroxidación debido al cumplimiento del programa.
El ejercicio se promueve generalmente como un método de control de peso, pero se pueden lograr beneficios significativos para la salud incluso cuando la pérdida de peso inducida por el ejercicio es menor a la esperada. King y col. informaron que de 58 sujetos con DMT2 que participaron en un programa de ejercicios, 26 no perdieron peso o incluso aumentaron de peso. Estos 26 sujetos «no respondedores» también mostraron cambios favorables significativos en el VO2max, la circunferencia de la cintura y la presión arterial26.
Del mismo modo en nuestro estudio, los participantes que no perdieron peso también mostraron beneficios en VO2max, MCP1 y TBARS. Debería ser conveniente considerar los beneficios del ejercicio no solo por la pérdida de peso corporal sino también por la mejoría de otros marcadores.
En conclusión, los pacientes con DMT1 se benefician de un programa de ejercicios simple y acompañado que los ayuda a mejorar la capacidad cardiorrespiratoria (VO2max) y a reducir los marcadores de inflamación y la peroxidación lipídica. Además, estas mejoras pueden ocurrir independientemente de las mejoras en la glucemia, y por lo tanto, tener una glucemia bien controlada y ser sedentario no es suficiente para prevenir complicaciones/comorbilidades en pacientes con DMT1.
Agradecimientos y fuentes de financiamiento
Este trabajo ha sido financiado a través de los subsidios otorgados (2013-2015) por la Secretaria de Ciencia, Tecnología y Postgrado, de la Universidad Nacional de Cuyo, Mendoza, Argentina.
Referencias
- Vaidya V, Gangan N, Sheehan J: Impact of cardiovascular complications among patients with Type 2 diabetes mellitus: a systematic review. Expert review of pharmacoeconomics & outcomes research 2015; 15(3): 487-497.
- Huxley RR, Peters SA, Mishra GD, Woodward M: Risk of all-cause mortality and vascular events in women versus men with type 1 diabetes: a systematic review and meta-analysis. The lancet Diabetes & endocrinology 2015; 3(3): 198-206.
- Berezin A: Metabolic memory phenomenon in diabetes mellitus: Achieving and perspectives. Diabetes & metabolic syndrome 2016; 10(2 Suppl 1): S176-183.
- de Ferranti SD, de Boer IH, Fonseca V, Fox CS, Golden SH, Lavie CJ, Magge SN, Marx N, McGuire DK, Orchard TJ et al. Type 1 diabetes mellitus and cardiovascular disease: A scientific statement from the American Heart Association and American Diabetes Association. Circulation 2014; 130(13): 1110-1130.
- Kolb H, Mandrup-Poulsen T. The global diabetes epidemic as a consequence of lifestyle-induced low-grade inflammation. Diabetologia 2010; 53(1):10- 20.
- Chillaron JJ, Benaiges D, Mane L, Pedro-Botet J, Flores Le-Roux JA. Obesity and type 1 diabetes mellitus management. Minerva endocrinologica 2015; 40(1): 53-60.
- Conway B, Miller RG, Costacou T, Fried L, Kelsey S, Evans RW, Orchard TJ. Temporal patterns in overweight and obesity in Type 1 diabetes. Diabet Med 2010; 27(4): 398-404.
- Polsky S, Ellis SL. Obesity, insulin resistance, and type 1 diabetes mellitus. Current opinion in endocrinology, diabetes, and obesity 2015; 22(4): 277- 282.
- Pinhas-Hamiel O, Levek-Motola N, Kaidar K, Boyko V, Tisch E, Mazor- Aronovitch K, Graf-Barel C, Landau Z, Lerner-Geva L, Frumkin Ben-David R. Prevalence of overweight, obesity and metabolic syndrome components in children, adolescents and young adults with type 1 diabetes mellitus. Diabetes/metabolism research and reviews 2015; 31(1): 76-84.
- Moreno PR, Murcia AM, Palacios IF, Leon MN, Bernardi VH, Fuster V, Fallon JT. Coronary composition and macrophage infiltration in atherectomy specimens from patients with diabetes mellitus. Circulation 2000; 102(18): 2180-2184.
- Hamad A, Qureshi HJ, Roohi N. Assessment of C-reactive proteins in recently diagnosed type-1 diabetic children as a risk marker of early atherosclerosis. Journal of Ayub Medical College, Abbottabad. JAMC 2014; 26(4): 434-436.
- Aravindhan V, Mohan V, Arunkumar N, Sandhya S, Babu S. Chronic Endotoxemia in Subjects with Type-1 Diabetes Is Seen Much before the Onset of Microvascular Complications. PloS one 2015; 10(9): e0137618.
- Boizel R, Bruttmann G, Benhamou PY, Halimi S, Stanke-Labesque F. Regulation of oxidative stress and inflammation by glycaemic control: evidence for reversible activation of the 5-lipoxygenase pathway in type 1, but not in type 2 diabetes. Diabetologia 2010; 53(9): 2068-2070.
- Ceriello A, Novials A, Ortega E, Canivell S, La Sala L, Pujadas G, Esposito K, Giugliano D, Genovese S. Glucagon-like peptide 1 reduces endothelial dysfunction, inflammation, and oxidative stress induced by both hyperglycemia and hypoglycemia in type 1 diabetes. Diabetes care 2013; 36(8): 2346-2350.
- Das P, Biswas S, Mukherjee S, Bandyopadhyay SK. Association of Oxidative Stress and Obesity with Insulin Resistance in Type 2 Diabetes Mellitus. Mymensingh Med J 2016; 25(1): 148-152.
- Domingueti CP, Dusse LM, Carvalho M, de Sousa LP, Gomes KB, Fernandes AP: Diabetes mellitus. The linkage between oxidative stress, inflammation, hypercoagulability and vascular complications. J Diabetes Complications 2016; 30(4): 738-745.
- Tran B, Oliver S, Rosa J, Galassetti P. Aspects of inflammation and oxidative stress in pediatric obesity and type 1 diabetes: an overview of ten years of studies. Experimental diabetes research 2012; 2012: 683-680.
- Belalcazar LM, Reboussin DM, Haffner SM, Hoogeveen RC, Kriska AM, Schwenke DC, Tracy RP, Pi-Sunyer FX, Ballantyne CM, Look ARG. A 1-year lifestyle intervention for weight loss in individuals with type 2 diabetes reduces high C-reactive protein levels and identifies metabolic predictors of change: From the Look AHEAD (Action for Health in Diabetes) study. Diabetes care 2010; 33(11): 2297-2303.
- Kasapis C, Thompson PD. The effects of physical activity on serum C-reactive protein and inflammatory markers: A systematic review. Journal of the American College of Cardiology 2005; 45(10): 1563-1569.
- Carpenter R, Gilleland D. Impact of an exercise program on adherence and fitness indicators. Appl Nurs Res 2016; 30: 184-186.
- Lee HH, Emerson JA, Williams DM. The Exercise-Affect-Adherence Pathway: An Evolutionary Perspective. Front Psychol 2016; 7: 1285.
- Morgan F, Battersby A, Weightman AL, Searchfield L, Turley R, Morgan H, Jagroo J, Ellis S. Adherence to exercise referral schemes by participants - what do providers and commissioners need to know? A systematic review of barriers and facilitators. BMC Public Health 2016; 16: 227.
- Heydari P, Varmazyar S, Nikpey A, Variani AS, Jafarvand M. Step Test: A method for evaluating maximum oxygen consumption to determine the ability kind of work among students of medical emergencies. Electronic physician 2017; 9(3): 4020-4026.
- Theodorou AA, Nikolaidis MG, Paschalis V, Sakellariou GK, Fatouros IG, Koutedakis Y, Jamurtas AZ. Comparison between glucose-6-phosphate dehydrogenase-deficient and normal individuals after eccentric exercise. Medicine and science in sports and exercise 2010; 42(6): 1113-1121.
- Moldoveanu AI, Shephard RJ, Shek PN. The cytokine response to physical activity and training. Sports medicine 2001; 31(2): 115-144.
- King NA, Hopkins M, Caudwell P, Stubbs RJ, Blundell JE. Beneficial effects of exercise: shifting the focus from body weight to other markers of health. Br J Sports Med 2009; 43(12): 924-927.
- Tielemans SM, Soedamah-Muthu SS, De Neve M, Toeller M, Chaturvedi N, Fuller JH, Stamatakis E. Association of physical activity with all-cause mortality and incident and prevalent cardiovascular disease among patients with type 1 diabetes: The EURODIAB Prospective Complications Study. Diabetologia 2013; 56(1): 82-91.
- Bohn B, Herbst A, Pfeifer M, Krakow D, Zimny S, Kopp F, Melmer A, Steinacker JM, Holl RW, Initiative DPV. Impact of Physical Activity on Glycemic Control and Prevalence of Cardiovascular Risk Factors in Adults With Type 1 Diabetes: A Cross-sectional Multicenter Study of 18,028 Patients. Diabetes care 2015; 38(8): 1536-1543.
- Wei M, Gibbons LW, Kampert JB, Nichaman MZ, Blair SN. Low cardiorespiratory fitness and physical inactivity as predictors of mortality in men with type 2 diabetes. Ann Intern Med 2000; 132(8): 605-611.
- Ploeger HE, Takken T, de Greef MH, Timmons BW. The effects of acute and chronic exercise on inflammatory markers in children and adults with a chronic inflammatory disease: A systematic review. Exerc Immunol Rev 2009; 15: 6-41.
- Ambarish V, Chandrashekara S, Suresh KP. Moderate regular exercises reduce inflammatory response for physical stress. Indian journal of physiology and pharmacology 2012; 56(1): 7-14.
- Xia M, Sui Z. Recent developments in CCR2 antagonists. Expert Opin Ther Pat 2009; 19(3): 295-303.
- Sell H, Dietze-Schroeder D, Kaiser U, Eckel J. Monocyte chemotactic protein-1 is a potential player in the negative cross-talk between adipose tissue and skeletal muscle. Endocrinology 2006; 147(5): 2458-2467.
- Fiorentino TV, Prioletta A, Zuo P, Folli F. Hyperglycemia-induced oxidative stress and its role in diabetes mellitus related cardiovascular diseases. Current pharmaceutical design 2013; 19(32): 5695-5703.
- Rochette L, Zeller M, Cottin Y, Vergely C. Diabetes, oxidative stress and therapeutic strategies. Biochimica et biophysica acta 2014; 1840(9): 2709- 2729.
- Wang X, Tao L, Hai CX. Redox-regulating role of insulin: The essence of insulin effect. Molecular and cellular endocrinology 2012; 349(2): 111-127.