Adenoma hipofisario ectópico del seno esfenoidal persistente tras cirugía manejado con tratamiento conservador
María Martínez G1*, Pablo Trincado A2, María Elena López A2.
Ectopic pituitary adenoma in the sphenoid sinus persistent after surgery managed with conservative treatment
1. Unidad de Endocrinología y Nutrición. Hospital de Barbastro. Huesca. España
2. Servicio de Endocrinología y Nutrición. Hospital Universitario Miguel Servet. Zaragoza. España.
*Correspondencia:
María Martínez García
mariamartinez1109@gmail.com
Teléfono: 974249000
Dirección: Carretera Nacional 240, s/n,
22300 Barbastro, Huesca. España
Recibido: 29-05-2020
Aceptado: 18-07-2020
Resumen: Los adenomas hipofisarios ectópicos (EPA) constituyen un reto diagnóstico, dada su escasa prevalencia y variada presentación en la que puede incluirse un síndrome de hipersecreción de hormonas hipofisarias. La clínica suele ser larvada e inespecífica, no presentan ninguna característica radiológica diferencial y el diagnóstico habitualmente es anatomopatológico. Sin embargo, a pesar de ser tumores benignos, pueden presentar un comportamiento agresivo, con invasión ósea y difícil resección completa, por lo que un diagnóstico de sospecha precoz podría resultar en un tratamiento más eficaz y con un menor número de complicaciones. Presentamos el caso de una paciente con un adenoma hipofisario ectópico silente en el seno esfenoidal con inmunohistoquímica positiva para Hormona de crecimiento (GH) y prolactina que presentaba restos tumorales tras la intervención quirúrgica y ha sido manejada con tratamiento médico conservado, con buenos resultados.
Palabras clave: Adenoma hipofisario; Cabergolina; Seno esfenoidal; Tumor ectópico.
Abstract: Ectopic pituitary adenomas constitute a diagnostic challenge, given their low prevalence and varied presentation in which a pituitary hormone hypersecretion syndrome may be included. Clinical symptoms are usually latent and nonspecific, they have no differential radiological characteristics and the diagnosis is usually anatomopathological. However, despite being benign tumors, they can exhibit aggressive behavior, with bone invasion and difficult complete resection, so a diagnosis of early suspicion could result in more effective treatment and fewer complications. We present the case of a patient with a silent ectopic pituitary adenoma in the sphenoid sinus with positive immunohistochemistry for Growth Hormone (GH) and prolactin who had tumor remnants after surgery and was managed with conservative medical treatment, with good results.
Keywords: Cabergoline; Ectopic tumor; Pituitary adenoma; Sphenoid sinus.
Mujer de 70 años, con antecedentes de hipertensión arterial, dislipemia e hipotiroidismo primario en tratamiento sustitutivo con levotiroxina. Acude a su médico por sensación de mareo e inestabilidad de larga evolución, con aumento de intensidad en los últimos meses, así como dolor peri orbitario derecho de un año de evolución, sin disminución de la agudeza visual, nauseas ni vómitos. La paciente no refería galactorrea ni presentaba fenotipo de acromegalia. Dada la persistencia de la clínica y la ausencia de mejoría tras tratamiento con sulpirida y betahistina, se solicita TAC cerebral, en el que se objetiva una ocupación del seno esfenoidal derecho, de morfología nodular, que podría corresponder a un pólipo.
La TAC de senos paranasales confirma una tumoración de 13x10x15 mm en seno esfenoidal derecho, en íntimo contacto con carótida interna supraclinoidea, con erosión de pared posterior de seno esfenoidal, sin invasión intracraneal.
Posteriormente, la resonancia magnética (RM) muestra una silla turca “parcialmente vacía”, elongación de la carótida interna derecha en el segmento cavernoso, y por delante de la elongación y de la silla turca, una formación nodular de partes blandas, isointensa en T1 y T2, de 13x10x10 mm. Su morfología es regular, estructura homogénea y se realza también de forma homogénea tras la inyección del contraste, con una base de implantación sobre el tabique interesfenoidal y crecimiento en el interior del seno esfenoidal derecho sin extensión hacia la silla turca ni senos cavernosos (Figura 1). Se decide resección endoscópica nasosinusal de la lesión realizando previa esfeinoidotomía.
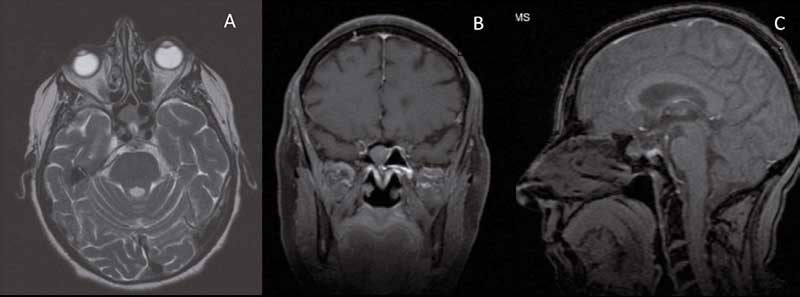 Figura 1: Resonancia magnética de senos paranasales con contraste. En corte axial (1A) se observa formación nodular, isointensa en T1 con el parénquima cerebral,
situada por delante de elongación de la arteria carótida derecha y de la silla turca. También se observa en corte coronal (1B), con base de implantación sobre el
tabique interesfenoidal y sin extensión a senos cavernosos, así como en corte sagital (1C), presentando crecimiento en el interior del seno esfenoidal derecho.
Figura 1: Resonancia magnética de senos paranasales con contraste. En corte axial (1A) se observa formación nodular, isointensa en T1 con el parénquima cerebral,
situada por delante de elongación de la arteria carótida derecha y de la silla turca. También se observa en corte coronal (1B), con base de implantación sobre el
tabique interesfenoidal y sin extensión a senos cavernosos, así como en corte sagital (1C), presentando crecimiento en el interior del seno esfenoidal derecho. El diagnóstico anatomopatológico fue de adenoma hipofisario ectópico, de 12 mm, que contactaba con bordes y con inmunohistoquímica positiva frente a prolactina y HGh- GH, además de a CKAE1-AE, CK8/18, CD56, cromogranina y sinaptofisina.
Es derivada a Endocrinología donde se realiza estudio hormonal hipofisario que no demuestra alteración: TSH 1,09 μU/mL (0,38-5,33), T4 Libre 0,75 ng/dL (0,58-1,64), LH 27,41 mUI/mL (postmenopausia 10,87- 58,64), FSH 86,25 mUI/ mL (postmenopausia 16,74-113,59), prolactina 8,91 ng/mL (2,74-19,64), cortisol 17,14 μgr/dL (5-25), ACTH 28,6 pg/mL (7,5-63,3), GH 0,028 ng/mL (0,01-3,607), IGF-1 86,5 ng/mL (35,1-216) y osmolaridad en orina 734 mOsm/kg (300-900).
A los 5 meses, la RM de control objetiva cambios postquirúrgicos sin poder descartar restos tumorales. Una gammagrafía con receptores de somatostatina 99mTc muestra una hipercaptación focal de intensidad superior a la esperable para la actividad fisiológica normal hipofisaria en la región del seno esfenoidal, anterior e inferior a hipófisis, donde se ubicaba el EPA, pudiendo corresponder a restos tumorales (Figura 2).

Figura 2: Gammagrafía de receptores de somatostatina con 99mTc. Se observa en ambas imágenes (2A y 2B) hipercaptación focal en región de seno esfenoidal derecho, anterior e inferior a hipófisis, en el territorio en el que se ubicaba el adenoma ectópico biopsiado, pudiendo corresponder a restos del adenoma ectópico.
Ante estos hallazgos, y dada la expresión de prolactina y GH en el tejido tumoral, se inicia tratamiento con cabergolina a dosis bajas (medio comprimido de 0.5 mg, 2 veces por semana) y somatulina 60 mg subcutánea profunda cada 28 días para evitar el crecimiento de restos tumorales, siendo este último suspendido por mala tolerancia. Actualmente la paciente se encuentra asintomática 30 meses después de la cirugía y no se ha objetivado crecimiento tumoral en los controles radiológicos realizados periódicamente.
Discusión
Los adenomas hipofisarios representan un 10% de los tumores cerebrales y suponen los tumores más habituales de la silla turca. Sin embargo, también se han descrito casos de adenomas hipofisarios ectópicos (EPA), definidos así cuando su crecimiento se produce fuera del área selar y sin continuidad con la glándula hipofisaria. Descritos por primera vez por Erdheim en 1909, su prevalencia es extremadamente baja, con 85 casos reportados en una revisión publicada en 20191. Este hecho, así como su muy variada presentación y la coexistencia de síndromes de hipersecreción hormonal, conllevan un difícil diagnóstico.
Se desconoce con exactitud el origen de la existencia de estos adenomas ectópicos, aunque se han propuesto varias explicaciones. La primera de ellas, y más aceptada, consiste en que constituyen una persistencia de células hipofisarias residuales tras el proceso de migración embrionaria de la bolsa de Rathke desde el techo faríngeo. Otra hipótesis relaciona su origen con la presencia de células aberrantes de la porción supra diafragmática del pars tuberalis ubicado en la región selar. Cualquiera de los dos supuestos explicaría que las localizaciones más habituales de EPA sean seno esfenoidal y región supraselar con un 34% cada una2,3, aunque es cierto que en una cuarta parte de los casos pueden presentarse también en otras localizaciones como clivus, nasofaringe, seno cavernoso y tercer ventrículo1,2. Otras posibles causas incluyen la presencia de células migratorias aberrantes del conducto craneofaríngeo (en el caso de los adenomas localizados en el tercer ventrículo) y la diseminación de un adenoma intraselar primario que, en rigor, no constituiría un verdadero EPA4. Por otra parte, no es descartable una predisposición genética como factor determinante en la transformación neoplásica de estas células, pues durante la embriogénesis se ha descrito un depósito de células fuera de la silla turca en el 75% de los cerebros normales5,6.
Su presentación clínica se correlaciona con la localización del tumor y el posible exceso de producción hormonal1. Las principales manifestaciones clínicas debidas a la localización incluyen cefalea en tumores del clivus, congestión sinusal si existe invasión del seno esfenoidal, epistaxis en los tumores nasofaríngeos y parálisis de un nervio craneal en los EPA del seno cavernoso7. En comparación con los de ubicación selar, se ha descrito un mayor porcentaje de tumores que presentan secreción hormonal, con evidencia inmunohistoquimica en un 85% y expresión clínica en un 50% de los casos1. Otros autores describen cifras similares, con un 75.6% de secreción hormonal en una serie de 75 casos revisados3. A diferencia de los eutópicos, en los que predominan los prolactinomas y los adenomas no funcionantes, en los EPA es más frecuente la producción de ACTH (37,2%), seguidos por prolactinomas (25,6%), adenomas inactivos (23,3%) y secretores de GH (10,5%)2,3,8. Curiosamente, además de ser más prevalente la secreción hormonal, también se ha descrito una relación con la localización, de forma que los tumores de seno esfenoidal son más propensos a producir ACTH, los del clivus, prolactina y los nasofaríngeos, TSH. Otra diferencia descrita con respecto a los adenomas eutópicos, tal y como sucede en el caso descrito, se relaciona con la mayor frecuencia de secreción bihormonal, incluyendo frecuentemente la TSH1. Por ello, ante la sospecha de un EPA, y dada la alta probabilidad de que sea funcionante, debería realizarse un estudio hormonal hipofisario completo.
Radiológicamente estos tumores pueden imitar otras lesiones de la base del cráneo, mostrándose isodensos o ligeramente hiperdensos en la TC7. La RM es útil para evaluar la extensión, la integridad de la duramadre y confirmar la presencia de glándula hipofisaria normal2, mostrándose isointensos en las imágenes T1 y con realce uniforme isointensos o ligeramente hiperintensos en T2, un patrón similar al observado en los meningiomas esfeno-orbitales7. Aunque se desconoce el mecanismo y a pesar de tratarse de tumores benignos, también se ha objetivado un comportamiento más agresivo en comparación con los localizados en la zona selar y presentando invasión ósea en más de un tercio de los casos, así como focos de necrosis y transformación maligna en 6 de 85 casos1. Debido a su escasa prevalencia, el diagnóstico preoperatorio es difícil de establecer, especialmente en los EPA no funcionantes asintomáticos, ya que los procedimientos diagnósticos habitualmente sugieren en primer lugar otro tipo de neoplasias, como cordomas, carcinoma nasofaríngeo, tumores salivales o tumor metastásico7,8,9.
Por tanto, para el diagnóstico de estos tumores se requiere el estudio histopatológico del tumor, incluyendo una inmunohistoquímica con marcadores neuroendocrinos y hormonas hipofisarias, siendo recomendable añadir al estudio estructural de las células tumorales un análisis genético o genómico adicional2,7. Generalmente están compuestos por células monomórficas cromofóbicas, sin atipia nuclear, de tamaño pequeño a mediano con reducido recuento mitótico y dispuestas en un patrón sinusoidal. El diagnóstico diferencial histológico incluye tumores carcinoides, carcinoma neuroendocrino, paraganglioma y carcinomas del tracto respiratorio superior8.
La transformación maligna es muy rara, y el tratamiento principal es la resección quirúrgica por lo que es fundamental un diagnóstico precoz, valorando la administración de radioterapia postoperatoria en los casos en los que la resección no puede realizarse o ha sido incompleta8. No obstante, algunos autores recomiendan de forma rutinaria realizar una evaluación hormonal en presencia de cualquier lesión paraselar, de modo que se pueda llevar a cabo un diagnóstico precoz y evitar en algunos casos una biopsia o una intervención quirúrgica. De hecho, en los últimos años, algunos casos de EPA productores de Prolactina, han sido eficazmente manejados con tratamiento médico con agonistas dopaminérgicos10, y EPAS productores de GH o TSH podrían beneficiarse de tratamientos con análogos de somatostatina11,12. Así, en el caso que presentamos, la evolución con tratamiento con cabergolina ha permitido una estabilización de la enfermedad, sin precisar nuevos tratamientos adicionales.
En conclusión, el EPA se debe tener en cuenta dentro del diagnóstico diferencial de los tumores de seno esfenoidal, siendo recomendable la realización de RM, así como biopsia esfenoidal previas al tratamiento quirúrgico, ya que pese a tratarse de tumores benignos, pueden presentar un comportamiento agresivo, con invasión ósea y difícil resección completa en los que un diagnóstico de sospecha precoz podría resultar en un tratamiento más eficaz y con menos complicaciones. En caso de comprobarse anatomopatológicamente la presencia de un EPA, debería realizarse un estudio hormonal completo y según los resultados, podría manejarse la posible persistencia o recidiva tumoral con tratamiento conservador según la secreción hormonal.
Conflicto de intereses
Los autores declaran que no hay conflicto de intereses.
Referencias
- Shuman W, Loewenstern J, Pai A, Bederson J, Shrivastava R. Variability in Clinical Presentation and Pathologic Implications of Ectopic Pituitary Tumors: Critical Review of Literature. World Neurosurg. 2019; 122: 397- 403. https://doi.org/10.1016/j.wneu.2018.10.200
- Ali R, Noma U, Jansen M, Smyth D. Ectopic pituitary adenoma presenting as midline nasopharyngeal mass. Ir J Med Sci 2010; 179: 593-595. DOI https://doi.org/10.1007/s11845-008-0236-x.
- Mitsuya K, Nakasu Y, Nioka H, Nakasu S. Ectopic growth hormonereleasing adenoma in the cabernous sinus. Neurol Med Chir (Tokyo) 2004; 44: 380-385.
- Pasquini E, Faustini-Fustini M, Sciarretta V, Saggese D, Roncaroli F, Serra D et al. Ectopic TSH-secreting pituitary adenoma of the vomerosphenoidal junction. Eur J Endocrinol 2003; 148: 253-257. https://doi.org/10.1530/ eje.0.1480253
- Ibarra-de la Torre A, Trujillo-Ojeda HM, Silva-Morales F, Ceballos-Arellano I, Acha-Herrera RE, Rivera-Salgado I, et al. Adenoma invasor en seno esfenoidal y clivus. Arch Neurocien (Mex) 2005; 10(3): 191-195.
- Hori A. Suprasellar peri-infundibular ectopic adenohypophysis in fetal and adult brains. J Neurosurg 1985; 63: 113-115.
- Wang H, Yu W, Zhang Z, Xu W, Zhang F, Bao W. Ectopic Pituitary Adenoma in the Spheno-Orbital Region. J Neuro-Ophthalmol 2010; 30: 135-137.
- Quitral R, Contreras JM. Adenoma ectópico hipofisiario: Reporte de un caso y revisión de la literatura. Rev. Otorrinolaringol. Cir. Cabeza Cuello 2008; 68: 295-300.
- Mizutani A, Yamaguchi-Okada M, Yokota N, Namba H. Asymptomatic non-functioning ectopic pituitary adenoma in the suprasellar region: A case report. B. J. Neurosurgery 2009; 23(3): 321-323.
- Agely A, Okromelidze L, Vilanilam GK, Chaichana KL, Middlebrooks EH, Gupta V. Ectopic pituitary adenomas: common presentations of a rare entity. Pituitary. 2019 Aug; 22(4): 339-343.
- Ortiz E, Peldoza M, Monnier E, Gejman R, Henriquez M, Barra MI, et al. Ectopic pituitary adenoma of the TSH-secreting sphenoidal sinus with excellent response to somatostatin analogs. Theory of the embryogenesis and literature review from a clinical case. Steroids. 2020 Feb; 154: 108535.
- Ramírez C, Hernández-Ramirez LC, Espinosa-de-los-Monteros AL, Franco JM, Guinto G, Mercado M. Ectopic acromegaly due to a GH-secreting pituitary adenoma in the sphenoid sinus: a case report and review of the literature. BMC Res Notes. 2013 Oct; 6(1): 411.